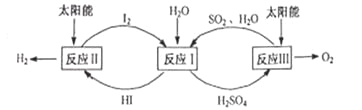
题目内容
【题目】结合下列图示装置。
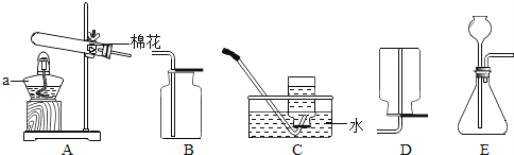
回答有关问题:
(1)仪器a的名称是_____.
(2)实验室用高锰酸钾制取氧气,可选择的发生装置是_____(填标号),试管口放一团棉花的作用是___;用装置C收集氧气,导管口开始有气泡放出时,不宜立即收集,理由是____;集满氧气的集气瓶应___ (填“正”或“倒”)放在桌上.
(3)实验室常用石灰石与稀盐酸反应制取二氧化碳,其反应的化学方程式是_________________;若用排空气法收集二氧化碳,收集装置应选用_____ (填标号).
【答案】 酒精灯 A; 防止加热时高锰酸钾粉末进入导管; 收集的氧气中混有空气; 正 CaCO3+2HCl═CaCl2+H2O+CO2↑ B
【解析】(1)仪器a是酒精灯。(2)加热固体制取气体,选择发生装置A,用高锰酸钾制取氧气,试管口放一团棉花的作用是防止加热时高锰酸钾粉末进入导管。导管口开始有气泡放出时,不宜立即收集,原因是此时收集的氧气中混有空气。由于氧气的密度比空气的密度大,所以集满氧气的集气瓶应正放在桌上。(3)实验室制取二氧化碳的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑,二氧化碳的密度比空气的密度大,用向上排空气法收集,故选B。

 备战中考寒假系列答案
备战中考寒假系列答案【题目】在学习第十单元《常见的酸和碱》时,九年级1班的同学按照老师的要求做了如图两个实验,①向盛有氢氧化钠溶液的试管中缓缓吹气,②向盛有氢氧化钠溶液的烧杯中滴加过量稀盐酸,结果都没有观察到明显现象。为此同学们分甲、乙两组开展了一系列探究活动。
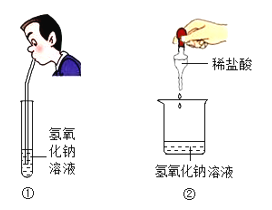
【提出问题】氢氧化钠溶液与二氧化碳和稀盐酸能发生反应吗?
【做出猜想】猜想一:不能发生反应。
猜想二:能发生反应但无明显现象。
【查阅资料】已知通常状况下,1体积的水约能溶解1体积的二氧化碳。
【实验探究】
(1)甲组:探究氢氧化钠溶液与二氧化碳能否发生化学反应。
方案一: 向①中得到的液体中滴加某溶液,观察到有气泡产生,说明氢氧化钠溶液能与二氧化碳发生反应,产生该现象的化学方程式是_________。
方案二: 向充满20ml二氧化碳的密闭注射器中注入3ml氢氧化钠溶液,观察到如图现象时,说明二者已反应。请你解释说明该方案是否严谨?________。
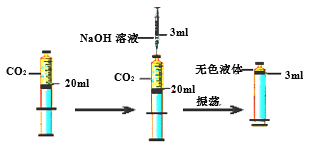
(2)乙组:探究氢氧化钠溶液与稀盐酸能否发生化学反应。乙组设计如下实验进行探究。
实验过程 | 实验现象 | 实验结论 | |
方案一 | 取②中得到溶液少许于试管中,滴加几滴硝酸银溶液 | _______ | 氢氧化钠溶液能与稀盐酸发生反应 |
方案二 | 取②中得到的溶液少许于试管中,滴加_______溶液 | 无明显现象 |
【反思与评价】
①通过交流,甲组认为乙组的方案一不太严谨,从微观角度解释原因________。
②乙组同学经过讨论交流后接受了甲组同学的建议,并采用了一种物理方法探究氢氧化钠溶液与稀盐酸反应有新物质生成,该方法可能是______。
【总结与提升】
愉快的探究之旅结束了,留给同学们的不仅仅是化学知识,更获得了解决问题的科学方法。对于无明显现象的化学变化,我们可以通过________的方法探究其反应是否发生。