题目内容
苹果酸是一种利用苹果发酵制成的饮料,具有一定的保健功能.苹果酸(化学式为C4H6O5)是这种饮料的有效成分.请你计算:(相对原子质量:H-1 O-16 C-12)(1)苹果酸中,碳、氢、氧三种元素的质量比(最简整数比)依次为______;
(2)若苹果酸中氢元素的质量分数为a%,则碳元素的质量分数为______(用含a的质量百分数表示)
(3)多少克苹果酸与88g二氧化碳所含碳元素的质量相等?(要求写出计算过程)
【答案】分析:(1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据氢元素的质量分数、氢碳元素的质量比进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:(1)苹果酸中,碳、氢、氧三种元素的质量比(最简整数比)依次为(12×4):(6×1):(16×5)=24:3:40.
(2)氢元素与碳元素的质量比为:(12×4):(6×1)=8:1,若苹果酸中氢元素的质量分数为a%,则碳元素的质量分数为8a%.
(3)设需要苹果酸的质量为x,
x× 100%=88g×
100%=88g×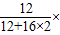 100% x=67g.
100% x=67g.
故答案为:(1)24:3:40;(2)8a%;(3)67g.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.
(2)根据氢元素的质量分数、氢碳元素的质量比进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:(1)苹果酸中,碳、氢、氧三种元素的质量比(最简整数比)依次为(12×4):(6×1):(16×5)=24:3:40.
(2)氢元素与碳元素的质量比为:(12×4):(6×1)=8:1,若苹果酸中氢元素的质量分数为a%,则碳元素的质量分数为8a%.
(3)设需要苹果酸的质量为x,
x×
 100%=88g×
100%=88g×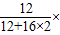 100% x=67g.
100% x=67g.故答案为:(1)24:3:40;(2)8a%;(3)67g.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目