题目内容
【题目】下图是氮气和氧气在放电条件下发生反应的微观模拟图,请回答问题: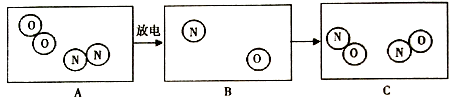
(1)请将B图补充完整,以使其正确:。
(2)该变化前后没有发生改变的粒子是。
(3)此反应的微观实质是: , 每一个氧原子和一个氮原子构成一个一氧化氮分子。
【答案】
(1)补充一个氮原子、一个氧原子
(2)氮原子、氧原子
(3)在放电的条件下,氮分子分解成氮原子、氧分子分解成氧原子
【解析】解:(1)、根据质量守恒定律可知:反应前后元素原子的质量和个数不变。故需补充:补充一个氮原子、一个氧原子;(2)、原子是化学变化中的罪行粒子。故该变化前后没有发生改变的粒子是:氮原子、氧原子(或“N、O” );(3)、化学变化的实质是:分子分成原子,原子又重新结合成新的分子。故此反应的微观实质是:在放电的条件下,氮分子分解成氮原子、氧分子分解成氧原子,每一个氧原子和一个氮原子构成一个一氧化氮分子。
所以答案是:补充一个氮原子、一个氧原子;氮原子、氧原子;在放电的条件下,氮分子分解成氮原子、氧分子分解成氧原子。

 名校课堂系列答案
名校课堂系列答案【题目】有关物质组成及化学规律的发现对化学的发展做出了重要贡献。
(1)法国化学家拉瓦锡为化学学科的发展做出了巨大贡献,下列有关发现与他有密切关系的是。
A.空气的组成
B.元素周期律
C.质量守恒定律
D.原子的结构
(2)【实验回顾】如图所示装置可用于粗略测定空气中氧气含量。
①集气瓶内加入少量水的作用是 ;
②红磷燃烧结束后,冷却至室温,打开弹簧夹,水能进入集气瓶中的原因是;
(3)【问题提出】有实验资料表明:燃烧过程中,当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测定结果与理论值误差较大。
【实验改进】
Ⅰ.根据铁在空气中生锈(铁与氧气、水发生缓慢氧化生成铁锈)的原理设计了图12所示的实验装置,再次测定空气中氧气含量。装置中饱和食盐水,活性炭会加速铁生锈。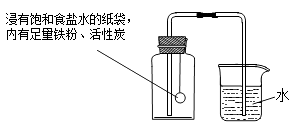
Ⅱ.测得实验数据如表
测量项目 | 实验前 | 实验后 | |
烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
体积/mL | 80.0 | 49.0 | 150.0 |
【交流表达】
根据表中数据计算,改进实验后测得的空气中氧气的体积分数是(计算结果精确到0.1%)。
(4)从实验原理角度分析,改进后的实验结果比前者准确度更髙的原因是:
①铁的缓慢氧化使集气瓶中的氧气消耗更彻底,使实验结果更准确。
②。
(5)【查阅资料】镁条除了和氧气反应,还可以和氮气、二氧化碳发生反应。
【问题拓展】镁条能在空气中燃烧,镁与氧气反应的化学方程式为。探究空气中氧气含量的实验中,若将燃烧匙中的药品换成镁粉,其它操作均正确,实验结束后,测量得到的结果(填“偏大”、“偏小”或“无影响”)。