题目内容
 实验室常用于制取氧气的方法有:a、加热氯酸钾晶体和二氧化锰粉末;b、加热高锰酸钾固体;c、用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生水和氧气.
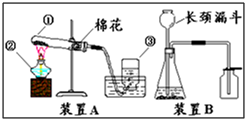
实验室常用于制取氧气的方法有:a、加热氯酸钾晶体和二氧化锰粉末;b、加热高锰酸钾固体;c、用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生水和氧气.(1)指出图中仪器的名称①
试管
试管
②酒精灯
酒精灯
请仔细分析装置A的特点,推测其所用的制氧气的方法是b
b
(填a、b或c)(2)采用方法c制取氧气应该选用装置
B
B
(填“A”或“B”),该反应的化学方程式为:2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
. 利用装置B制氧气时,长颈漏斗的下端要插入液面以下,其目的是
| ||
防止气体从长颈漏斗逸出(合理即可)
防止气体从长颈漏斗逸出(合理即可)
.(3)利用装置A制氧气,A中发生的反应的化学方程式:
2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
,在结束实验时要先撤离导管出水面,再熄灭酒精灯,其目的是
| ||
防止水倒吸炸裂试管(合理即可)
防止水倒吸炸裂试管(合理即可)
;(4)比较a、b、c三种制取氧气的方法,最好选用方法的是
c
c
,原因是:不需加热(或操作简便,答案合理即可)
不需加热(或操作简便,答案合理即可)
.分析:(1)依据常用仪器回答;装置A是加入固体制取氧气的方法,加入高锰酸钾制取氧气试管口要放棉花,据此分析解答;
(2)用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生水和氧气,不需加热,属于固液常温型,故选B;并据反应原理书写方程式;长颈漏斗下端要插入液面以下是为了防止气体从长颈漏斗逸出;
(3)依据反应原理书写方程式;实验结束要先移导管后熄灯,防止水倒吸引起试管炸裂;
(4)比较三种制取氧气的方法,可从是否需要加热、操作是否简便等方面进行评价.
(2)用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生水和氧气,不需加热,属于固液常温型,故选B;并据反应原理书写方程式;长颈漏斗下端要插入液面以下是为了防止气体从长颈漏斗逸出;
(3)依据反应原理书写方程式;实验结束要先移导管后熄灯,防止水倒吸引起试管炸裂;
(4)比较三种制取氧气的方法,可从是否需要加热、操作是否简便等方面进行评价.
解答:解:(1)依据常用仪器,图中仪器是试管和酒精灯;装置A是加入固体制取氧气的方法,且试管口有棉花,说明是用加热高锰酸钾的方法制取氧气;
故答案为:试管;酒精灯;b;
(2)用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生水和氧气,不需加热,属于固液常温型,故选B,方程式是2H2O2
2H2O+O2↑;长颈漏斗下端要插入液面以下是为了防止气体从长颈漏斗逸出;
故答案为:B;2H2O2
2H2O+O2↑;防止气体从长颈漏斗逸出(合理即可);
(3)由(1)分析可知,装置A是用高锰酸钾制取氧气,高锰酸钾加热生成锰酸钾、二氧化锰和氧气,方程式是2KMnO4
K2MnO4+MnO2+O2↑;实验结束要先移导管后熄灯,防止水倒吸引起试管炸裂;
故答案为:2KMnO4
K2MnO4+MnO2+O2↑;防止水倒吸炸裂试管(合理即可);
(4)氯酸钾、高锰酸钾制取氧气需要加热,过氧化氢制取氧气常温反应就可以,所以具有不需加热,节约能源,操作简便等优点;
故答案为:c;不需加热(或操作简便,答案合理即可).
故答案为:试管;酒精灯;b;
(2)用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生水和氧气,不需加热,属于固液常温型,故选B,方程式是2H2O2
| ||
故答案为:B;2H2O2
| ||
(3)由(1)分析可知,装置A是用高锰酸钾制取氧气,高锰酸钾加热生成锰酸钾、二氧化锰和氧气,方程式是2KMnO4
| ||
故答案为:2KMnO4
| ||
(4)氯酸钾、高锰酸钾制取氧气需要加热,过氧化氢制取氧气常温反应就可以,所以具有不需加热,节约能源,操作简便等优点;
故答案为:c;不需加热(或操作简便,答案合理即可).
点评:掌握实验室制取氧气的方法,并会应用装置选取方法及相关知识分析和解决问题是解答的关键.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
 实验室常用于制取氧气的方法有:
实验室常用于制取氧气的方法有: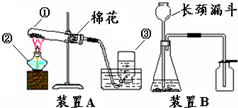 实验室常用于制取氧气的方法有:a、加热氯酸钾晶体和二氧化锰粉末;b、加热高锰酸钾固体;c、用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生水和氧气.
实验室常用于制取氧气的方法有:a、加热氯酸钾晶体和二氧化锰粉末;b、加热高锰酸钾固体;c、用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生水和氧气. 实验室常用于制取氧气的方法有:
实验室常用于制取氧气的方法有: