题目内容
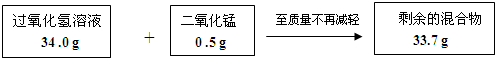
某同学为了测定一瓶过氧化氢溶液中溶质的质量分数,取该溶液30g,加入二氧化锰0.5g,完全反应后,称得烧杯内剩余物质的总质量为29.7g.请回答下列问题:
(1)二氧化锰在反应中的作用是 .
(2)计算该过氧化氢溶液中溶质的质量分数.(请列式计算)
(3)现要配制100g溶质质量分数为3%的过氧化氢消毒液,需12%过氧化氢溶液的质量为 g.
(1)二氧化锰在反应中的作用是
(2)计算该过氧化氢溶液中溶质的质量分数.(请列式计算)
(3)现要配制100g溶质质量分数为3%的过氧化氢消毒液,需12%过氧化氢溶液的质量为
考点:根据化学反应方程式的计算,用水稀释改变浓度的方法,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据催化剂的作用分析;
(2)根据过氧化氢分解的方程式及质量守恒定律,求出生成的氧气的质量,由氧气的质量求出过氧化氢溶液中溶质质量,再求出溶质的质量分数;
(3)根据溶质质量不变进行计算.
(2)根据过氧化氢分解的方程式及质量守恒定律,求出生成的氧气的质量,由氧气的质量求出过氧化氢溶液中溶质质量,再求出溶质的质量分数;
(3)根据溶质质量不变进行计算.
解答:解:(1)反应前后二氧化锰的质量和化学性质都没改变,二氧化锰为反应的催化剂,反应中起催化作用;
(2)生成O2的质量=30g+0.5g-29.7g=0.8g;
设该过氧化氢溶液中溶质的质量为x
2H2O2
2H2O+O2↑
68 32
x 0.8g
=
解得:x=1.7g
该溶液中溶质的质量分数为:
×100%=5.7%;
(3)根据加水稀释前后溶质质量不变,需12%溶液的质量
=25g
故答案为:(1)催化作用; (2)过氧化氢溶液中溶质的质量分数5.7%;(3)25.
(2)生成O2的质量=30g+0.5g-29.7g=0.8g;
设该过氧化氢溶液中溶质的质量为x
2H2O2
| ||
68 32
x 0.8g
| 68 |
| x |
| 32 |
| 0.8g |
解得:x=1.7g
该溶液中溶质的质量分数为:
| 1.7g |
| 30g |
(3)根据加水稀释前后溶质质量不变,需12%溶液的质量
| 100g×3% |
| 12% |
故答案为:(1)催化作用; (2)过氧化氢溶液中溶质的质量分数5.7%;(3)25.
点评:本题主要考查学生运用化学方程式和溶质质量分数和质量守恒定律综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
目前许多地区空气污染指数超标,其中不会造成空气污染的因素是( )
| A、矿物燃烧后排放出SO2等有害气体 |
| B、植物的光合作用 |
| C、汽车尾气未经处理排放到空气中 |
| D、大量植被破坏形成沙尘暴 |
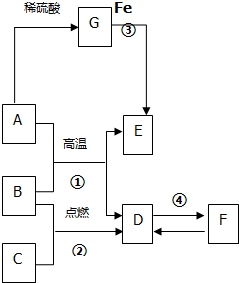 如图A~G是初中化学常见的物质,其中A为黑色固体,E为红色固体单质,B、C、D均为无色气体,F为石灰石的主要成分,G为蓝色溶液,请根据如图回答下列问题:
如图A~G是初中化学常见的物质,其中A为黑色固体,E为红色固体单质,B、C、D均为无色气体,F为石灰石的主要成分,G为蓝色溶液,请根据如图回答下列问题: