题目内容
已知草酸(H2C2O4)固体与浓硫酸供热发生化学反应:H2C2O4
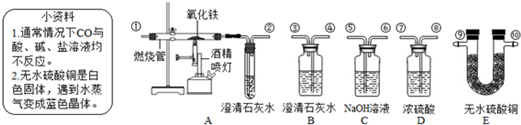
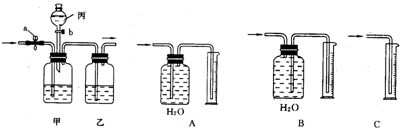
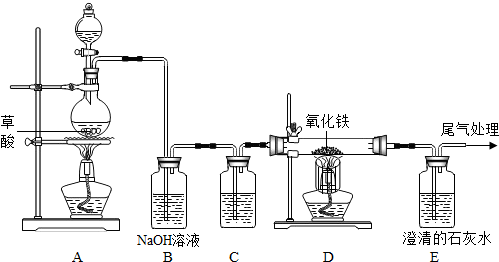
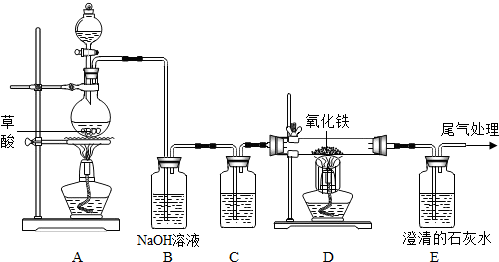
CO2↑+CO↑+H2O.某化学兴趣小组同学设计如下实验装置,用于制取纯净干燥的CO气体来还原氧化铁.请根据题目要求回答下列问题:(已知CO2+2NaOH=Na2CO3+H2O,浓硫酸具有强烈的吸水性)
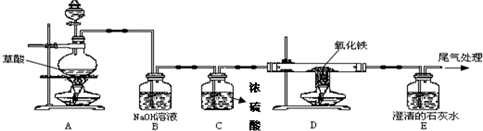
(1)实验开始时,应首先点燃
(2)装置B中NaOH的作用是
(3)D装置玻璃管中观察的现象是
(4)E处能够观察到澄清石灰水变浑浊,发生的化学方程式为
| ||
| △ |

(1)实验开始时,应首先点燃
A
A
处的酒精灯(填装置序号).(2)装置B中NaOH的作用是
除去(或吸收)二氧化碳
除去(或吸收)二氧化碳
.(3)D装置玻璃管中观察的现象是
红色粉末逐渐变为黑色
红色粉末逐渐变为黑色
,反应的化学方程式为Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
.
| ||
(4)E处能够观察到澄清石灰水变浑浊,发生的化学方程式为
CO2+Ca(OH)2=CaCO3↓+H2O
CO2+Ca(OH)2=CaCO3↓+H2O
;从E装置出来的尾气要进行处理,是因为尾气中含有CO(或一氧化碳)
CO(或一氧化碳)
.分析:(1)一氧化碳还原氧化铁首先要通一氧化碳排尽管内空气,防止加热发生爆炸,所以要先点燃A处酒精灯,制取一氧化碳;
(2)要制取纯净干燥的一氧化碳,可用氢氧化钠溶液除二氧化碳;
(3)一氧化碳可与红色的氧化铁反应生成黑色的铁粉,同时生成二氧化碳,据此分析解答;
(4)二氧化碳使澄清石灰水变浑浊,一氧化碳有毒,排放到空气中会造成大气污染,所以必须对尾气进行处理.
(2)要制取纯净干燥的一氧化碳,可用氢氧化钠溶液除二氧化碳;
(3)一氧化碳可与红色的氧化铁反应生成黑色的铁粉,同时生成二氧化碳,据此分析解答;
(4)二氧化碳使澄清石灰水变浑浊,一氧化碳有毒,排放到空气中会造成大气污染,所以必须对尾气进行处理.
解答:解:(1)为了防止发生爆炸,点燃或加热可燃性气体都必须验纯,故应利用生成的一氧化碳排净装置内的空气,应该先点燃A处的酒精灯;
(2)因为要制取纯净干燥的一氧化碳,B装置内是氢氧化钠能吸收产生的二氧化碳,得到纯净的一氧化碳;
(3)装置D中一氧化碳和氧化铁反应生成铁和二氧化碳,故玻璃管中观察的现象是 红色粉末逐渐变为黑色,反应的方程式为:Fe2O3+3CO
2Fe+3CO2;
(4)二氧化碳和澄清石灰水反应生成碳酸钙沉淀和水,反应方程式是:CO2+Ca(OH)2=CaCO3↓+H2O;一氧化碳有毒,过程中可能一氧化碳过多,必须对尾气进行处理;
故答案为:(1)A;
(2)除去(或吸收)二氧化碳;
(3)红色粉末逐渐变为黑色;Fe2O3+3CO
2Fe+3CO2;
(4)CO2+Ca(OH)2=CaCO3↓+H2O; CO (或一氧化碳).
(2)因为要制取纯净干燥的一氧化碳,B装置内是氢氧化钠能吸收产生的二氧化碳,得到纯净的一氧化碳;
(3)装置D中一氧化碳和氧化铁反应生成铁和二氧化碳,故玻璃管中观察的现象是 红色粉末逐渐变为黑色,反应的方程式为:Fe2O3+3CO
| ||
(4)二氧化碳和澄清石灰水反应生成碳酸钙沉淀和水,反应方程式是:CO2+Ca(OH)2=CaCO3↓+H2O;一氧化碳有毒,过程中可能一氧化碳过多,必须对尾气进行处理;
故答案为:(1)A;
(2)除去(或吸收)二氧化碳;
(3)红色粉末逐渐变为黑色;Fe2O3+3CO
| ||
(4)CO2+Ca(OH)2=CaCO3↓+H2O; CO (或一氧化碳).
点评:本题考查了炼铁的原理、实验现象、尾气处理以及应用.要注意有毒气体不能随意排放,可燃性气体在加热或点燃前的验纯,以及净化气体的方法.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目