题目内容
【题目】含碳酸钙80%的石灰石125g ,向其中加入足量稀盐酸恰好完全反应(假设除碳酸钙外的其他杂质都不溶于水,且不与稀盐酸反应),
求:⑴二氧化碳质量
⑵二氧化碳体积为多少升?(此状态下二氧化碳的密度约为2.0克/升)(保留一位小数)
【答案】(1)44g (2)22L
【解析】
试题分析:(1)设生成二氧化碳的质量为X
CaCO3+2HCl==CaCl2+H2O+CO2↑
100 44
80%×125g X
100::4=80%×125g:X
X=44g
(2)根据公式密度=质量/体积;得到V=m/p=44g/2g/l=22L

【题目】金属用途广泛,其结构和性质等是化学的重要研究内容。
(1)下图是铝的原子结构示意图。下列说法不正确的是 。
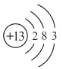
A.铝原子的质子数为13
B.在化合物中铝通常显+3价
C.铝是地壳中含量最多的元素
D.铝可作导线是由于它具有良好的导电性
(2)某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了下图实验,并对溶液A和固体B的成分进行了分析和实验探究。
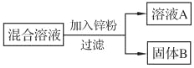
【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】①只有Zn(NO3)2
②Zn (NO3)2、AgNO3
③Zn (NO3)2、Cu(NO3)2
④Zn (NO3)2、AgNO3、Cu(NO3)2
【交流讨论】不合理的猜想是 (填标号),其理由是 。
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整。
实验步骤 | 现 象 | 有关反应的化学方程式 |
取少量固体B, 滴加 | 有气泡产生 |
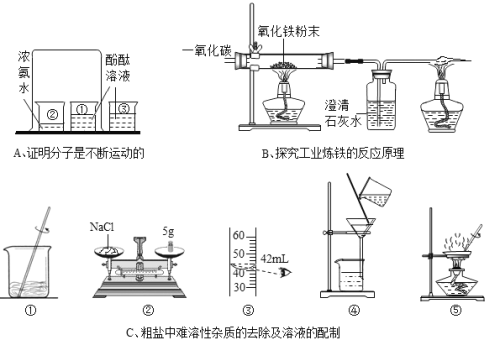
(3)下图是工业炼铁示意图。其中,焦炭的作用是燃烧提供能量和 ;有铁生成的化学方程式为 。
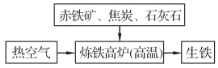
(4)某工厂利用废铁屑与废硫酸起反应来制取硫酸亚铁。现有废硫酸49 t(H2SO4的质量分数为10%),与足量废铁屑起反应,可生产硫酸亚铁的质量是多少?