题目内容
将家庭生活中的四种调味品分别取少量放入水中,不能形成溶液的是( )
A.蔗糖 B.白醋 C.食盐 D.花生油
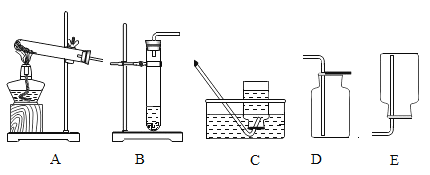
化学兴趣小组为验证质量守恒定律,做镁条在空气中燃烧的实验(如图1)。同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体。

(1)镁条燃烧的化学方程式是_____;
(2)同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量。小马认为这个反应不遵循质量守恒定律。你_____(“同意”或“不同意”)他的观点。你认为出现这样实验结果的原因可能是_____。
(3)小红按如图2装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体。
(提出问题)黄色固体是什么?
(查阅资料)①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)
固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
(做出猜想)黄色固体是Mg3N2
(实验探究)请设计实验,验证猜想
实验操作 | 实验现象 | 实验结论 |
将收集到的黄色固体放入试管中,加入适量的_____,在试管口放置湿润红色石蕊试纸。 | ①_____; ②_____。 | 黄色固体是Mg3N2 |
(反思与交流)空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是_____。
20 ℃时,四个实验小组分别取不同质量的NaCl,逐渐加入到各盛有50 g水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量剩余NaCl的质量。记录数据如表:
实验小组 | 第一组 | 第二组 | 第三组 | 第四组 |
所取NaCl的质量/g | 15 | 20 | 25 | 30 |
剩余NaCl的质量/g | 0 | 2 | 7 | 12 |
下列说法错误的是
A.20℃时,氯化钠的溶解度为18 g
B.二、三、四组溶液中溶质的质量分数相同
C.第二组所得溶液的溶质与溶剂的质量比为9∶25
D.相同温度下,NaCl在水里的溶解度与水的质量无关




 B.
B. C.
C. D.
D.