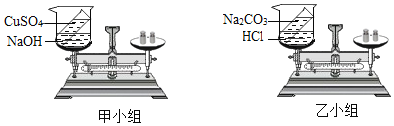
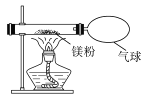
��Ŀ����
����Ŀ��ij��ѧ��ȤС���������Ʊ����ռ�չ���о�����ش��������⡣
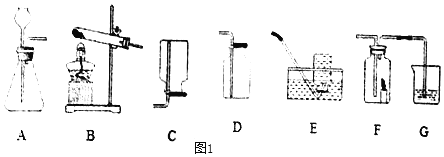
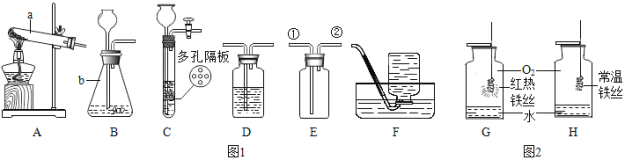
��1��ʵ�����ø��������ȡ�����ķ���װ����______����װ����ĸ��ţ����÷�Ӧ�Ļ�ѧ����ʽΪ______��
��2��ѡ�������ռ�����ʱ�����뿼�ǵ�����������______������ţ���
����ɫ ���ܶ� ����ȼ�� ���ܽ���
��3��ijͬѧ����A��F����ʵ�飬A������ҩƷ��ͬ��G��װ����ɫʯ����Һ��
����ʵ��ʱF������Ϩ��G����Һ��죬��A�з�Ӧ���������������______��д��ѧʽ����
����ʵ��ʱF������ȼ�ո�������A�з�Ӧ�Ļ�ѧ����ʽΪ______��
������ע�����滻����©�����ŵ���______��
��С�����Ʊ����ռ�һ���������塣�����������£�
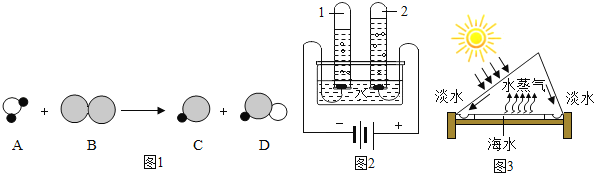
�����ϣ���ʵ���ҿ�����ϡ������ͭ�۷�Ӧ��ȡһ����������
��һ��������һ����ɫ���壬�ܶȽӽ�����
��һ�������ڳ�������Ѹ����������Ӧ�����غ�ɫ������������
��һ����������ˮ��������̼������������Һ�����ʷ�����Ӧ
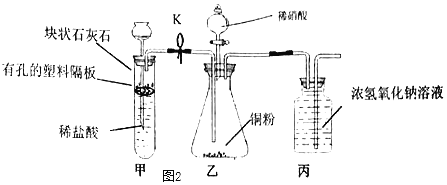
��4����С��տ�ʼ�����ȡʵ�鷽��ʱ��δ���Ӽ�װ�ã��ر�ֹˮ��K������װ���г�����______����֤���÷������ܻ��һ���������壨����̨�ȸ���װ����ʡ�ԣ���
��5����С��Ľ�ʵ�鷽���������ϼ�װ�á����ü��з�Ӧ����һ��ʱ�䣬�ر�ֹˮ�к��������е���ϡ���ᣬ���ܹ��ڱ����ռ���һ����������С����Ʒ������Ӽ�װ�õ�������______��ѡ���װ�ö���ѡ��ͼ1��Aװ�����ӵ���װ���ϣ�����Ϊѡ���װ�õ��ŵ�______��
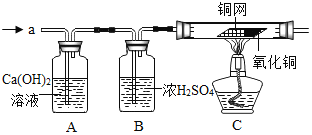
��6������Ϊ��װ����Ũ����������Һ�������ǣ����ٴ����㣩______��______��
���𰸡�B 2KMnO4![]() K2MnO4+MnO2+O2�� �ڢ� CO2 2H2O2
K2MnO4+MnO2+O2�� �ڢ� CO2 2H2O2![]() 2H2O+O2�� ���Կ��Ʒ�Ӧ������ ��ƿ�ڲ����غ�ɫ���� �ų���װ���ڵ����� �ر�ֹˮ�п����ü��з�Ӧֹͣ ��ֹ���ɵ�һ������������е������Ӵ� ���ն�����̼
2H2O+O2�� ���Կ��Ʒ�Ӧ������ ��ƿ�ڲ����غ�ɫ���� �ų���װ���ڵ����� �ر�ֹˮ�п����ü��з�Ӧֹͣ ��ֹ���ɵ�һ������������е������Ӵ� ���ն�����̼
��������
�⣺��1������ø����������������Ҫ���ȣ�����������ȷֽ���������غͶ������̺�������Ҫע����ƽ���ʴ�Ϊ��B��2KMnO4![]() K2MnO4+MnO2+O2����
K2MnO4+MnO2+O2����
��2��ѡ�������ռ�����ʱ�����뿼�ǵ����������У����ܶ����ܽ��ԣ��ʴ�Ϊ���ڢ���
��3��ijͬѧ����A��F����ʵ�飬A������ҩƷ��ͬ��G��װ����ɫʯ����Һ������ʵ��ʱF������Ϩ��G����Һ��죬��A�з�Ӧ��������������Ƕ�����̼������ʵ��ʱF������ȼ�ո�������A�в����������������������ڶ�������������������������ˮ��������Ҫע����ƽ��������ע�����滻����©�����ŵ��ǣ����Կ��Ʒ�Ӧ�����ʣ��ʴ�Ϊ����CO2����2H2O2![]() 2H2O+O2���������Կ��Ʒ�Ӧ�����ʣ�
2H2O+O2���������Կ��Ʒ�Ӧ�����ʣ�
��4����С��տ�ʼ�����ȡʵ�鷽��ʱ��δ���Ӽ�װ�ã��ر�ֹˮ��K������װ���г�������ƿ�ڲ����غ�ɫ��������֤���÷������ܻ��һ���������壻�ʴ�Ϊ����ƿ�ڲ����غ�ɫ���壻
��5����С����Ʒ������Ӽ�װ�õ������ǣ��ų���װ���ڵ�������ѡ���װ�ö���ѡ��ͼ1��Aװ�����ӵ���װ���ϣ�����Ϊѡ���װ�õ��ŵ㣺�ر�ֹˮ�п����ü��з�Ӧֹͣ���ʴ�Ϊ���ų���װ���ڵ��������ر�ֹˮ�п����ü��з�Ӧֹͣ��
��6����װ����Ũ����������Һ�������ǣ���ֹ���ɵ�һ������������е������Ӵ������ն�����̼�ȣ��ʴ�Ϊ����ֹ���ɵ�һ������������е������Ӵ������ն�����̼��