题目内容
【题目】称取铜、锌混合物粉末10.0 g置于烧杯中,慢慢加入稀硫酸使其充分反应,直至固体质量不再减少为止,此时用去49.0 g稀硫酸。剩余固体3.5 g。
(1)该混合物粉末中铜的质量分数为多少?
(2)充分反应后生成氢气的质量是多少?
【答案】
(1)
根据金属活动性顺序可知,金属铜不与稀硫酸反应,故反应剩余固体3.5g即为铜的质量,故该混合物粉末中铜的质量分数为:![]()
(2)
混合物中锌粉的质量为10.0g-3.5g=6.5g
设充分反应后生成氢气的质量是x
Zn+H2SO4=ZnSO4+H2↑
65 2
6.5g x![]()
解得x=0.2g
【解析】
(1)根据金属活动性顺序可知,金属铜不与稀硫酸反应,故反应剩余固体3.5g即为铜的质量,故该混合物粉末中铜的质量分数为:![]()
(2)混合物中锌粉的质量为10.0g-3.5g=6.5g
设充分反应后生成氢气的质量是x
Zn+H2SO4=ZnSO4+H2↑
65 2
6.5g x![]()
解得x=0.2g
根据金属的活动性,分析题中所发生的反应,判断出所余固体为铜,此为本题的突破口。

 名校课堂系列答案
名校课堂系列答案【题目】某校化学兴趣小组,在实验室里用二氧化锰和浓盐酸在加热条件下制取氯气并进行有关氯气性质的实验探究(如图所示).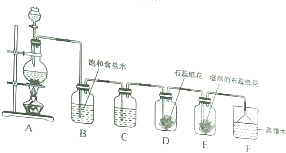
回答下列问题:
(1)从分液漏斗中加入的药品是 .
(2)从反应物的状态和反应条件考虑,装置A属于型气体发生装置.
(3)若进入装置D中的氯气是纯净干燥的,则装置B的作用是 , 装置C中盛有的溶液是 .
(4)实验过程中,同学们看到装置D中“石蕊纸花”(用石蕊溶液染成的紫色的干燥纸花,下同)无明显变化,E中湿润的石蕊纸花先变红后褪色.对此,同学们产生了浓厚的兴趣,于是继续进行以下实验探究.
【查阅资料】Ⅰ.氯气(Cl2)是一种黄绿色的有毒气体,能溶于水(溶解性不大),并能与水反应:Cl2+H2O═HCl+HClO(次氯酸).
Ⅱ.氯气溶于水所得的溶液成为氯水,氯水除了具有消毒作用,还具有漂白作用.
【提出问题】氯水中的什么物质具有漂白作用?
【提出猜想】猜想1:氯水中的H2O具有漂白作用.
猜想2:氯水中的HCl具有漂白作用.
猜想3:氯水中的HClO具有漂白作用.
猜想4:氯水中的Cl2具有漂白作用.
【实验探究】
实验操作 | 实验现象 | 结论 |
①将石蕊纸花放入水中 | 石蕊纸花 | 猜想1不成立 |
②将石蕊纸花放入中 | 石蕊纸花变红但不褪色 | 猜想2不成立 |
③ | 石蕊纸花先变红后褪色 | 猜想3 |
(5)【反思交流】①同学们一致认为,不用再做实验对猜想4进行探究,理由是:进行氯气性质的实验探究时,装置(填装置序号)的现象已证明了Cl2不具有漂白作用.
②钱程同学认为,由于氯气在水中的溶解性不大,用实验装置F中的蒸馏水吸收氯气效果不是很理想,于是将装置F中的蒸馏水换成了氢氧化钠溶液,则最终反应所得溶液中含有的盐类物质是 .

