题目内容
【题目】某厂排放的废水中含有碳酸钠,易造成环境污染.化学兴趣小组为该厂设计废水处理和利用的方案,进行了如下实验:取过滤后的水样200g,逐滴加入稀盐酸至恰好不再产生气体为止,反应过程中生成气体与所加稀盐酸的质量关系如图所示.回答下列问题(不考虑水样中杂质的影响):
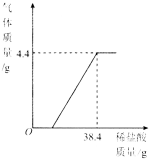
(1)反应生成CO2气体的质量是________g.
(2)反应后生成氯化钠的质量是多少?(写出计算过程)
(3)农业上常用10%~20%的氯化钠溶液来选种.请通过列式计算判断:上述实验恰好完全反应后所得溶液能否直接用于农业上选种?
【答案】(1)4.4
(2)11.7g
(3)不能直接用于农业上选种
【解析】水样中加入稀盐酸反应的化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑.(1)随着稀盐酸的加入,生成CO2的质量逐渐增大,当Na2CO3完全反应时,CO2的质量不再增加,根据图像可知,当加入38.4g稀盐酸时,生成CO2的质量达到最大值4.4g.
(2)根据CO2的质量,利用化学方程式即可求出生成氯化钠的质量为11.7g.(3)根据质量守恒定律,所得溶液质量为200g+38.4g-4.4g=234g,则反应后所得溶液中溶质质量分数为11.7g/234g×100%=5%,显然,该溶液不能直接用于农业上选种.
(1)4.4
(2)解:设反应后生成氯化钠的质量为x.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
117 44
x 4.4g
117︰44=x︰4.4g
x=11.7g
答:反应后生成氯化钠的质量为11.7g
(3)反应后溶液质量为200g+38.4g-4.4g=234g
反应后溶液中溶质的质量分数为11.7g/234g×100%=5%<10%,故不能直接用于农业上选种.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目