题目内容
【题目】某小组用传感器探究氢氧化钠溶液和稀盐酸反应过程中温度和pH的变化。
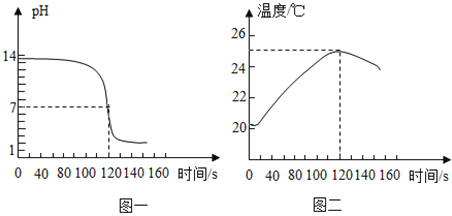
(1)根据图一可知该实验是将_____溶液摘入_____溶液中。
(2)根据图二可知中和反应是_____反应(选填“吸热”或“放热”),最终所得溶液的溶质是_____(用化学式表示)。
(3)依据以上实验,说法正确的是_____。
A 实验中NaCl的质量分数一直在变大
B 实验中H2O的质量一直在变大
C 一段时间后,溶液pH一定会变为0
D 选用pH试纸也可以证明两者能发生化学反应
(4)现有5%的氢氧化钠溶液16g,当pH=7时,求消耗的稀盐酸溶质的物质的量。_____(根据方程式进行计算)
【答案】稀盐酸 氢氧化钠 放热 NaCl、HCl BD 0.02mol
【解析】
(1)根据图一可知该实验是将稀盐酸溶液摘入氢氧化钠溶液中,这是因为随着反应进行,溶液pH由大于7逐渐减小。
故填:稀盐酸;氢氧化钠。
(2)根据图二可知过程中温度升高,因此中和反应是放热反应,最终所得溶液显酸性,即盐酸过量,溶质是NaCl、HCl。
故填:放热;NaCl、HCl。
(3)A.完全反应后继续加入稀盐酸,氯化钠质量分数变小,该选项说法不正确;
B.实验中反应生成水,溶液中的溶剂是水,因此H2O的质量一直在变大,该选项说法正确;
C.一段时间后,溶液pH不一定会变为0,该选项说法不正确;
D.选用pH试纸也可以证明两者能发生化学反应,这是因为氢氧化钠溶液pH大于7,恰好和稀盐酸反应pH等于7,盐酸过量时pH小于7,该选项说法正确。
故填:BD。
(4)氢氧化钠的物质的量为:![]() ,设消耗的稀盐酸溶质的物质的量为x,则
,设消耗的稀盐酸溶质的物质的量为x,则
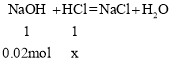
![]()
x=0.02mol,
答:消耗的稀盐酸溶质的物质的量是0.02mol。

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目