题目内容
书写下列化学符号:(1)过氧化氢制取氧气
(2)高锰酸钾制取氧气
(3)原子得失电子就变成 ,带正电的离子叫 ,带负电的离子叫 ,NaCl由 和 构成
(4)标出加点元素符号的化合价:
 K
K O4
O4  H4
H4 O3
O3(5)完全电解X克水能得到5ml氧气,同时得到氢气为 ml.
(6)单质的化合价为 .
(7)地壳中含量最多的元素是 最多的金属元素 .
【答案】分析:本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答:解:(1)过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2 2H2O+O2↑.
2H2O+O2↑.
(2)高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式是2KMnO4 K2MnO4+MnO2+O2↑.
K2MnO4+MnO2+O2↑.
(3)原子得失电子后变成离子,带正电的离子叫阳离子,带负电的离子叫阴离子,NaCl是由Na+和Cl-构成的;
(4)根据在化合物中正负化合价代数和为零,可知:CO2中C元素的化合价为:a+(-2)×2=0,则a=+4;
KMnO4中Mn的元素化合价为:(+1)+b+(-2)×4=0,则b=+7;
铵根的化合价为+1价,硝酸根的化合价为-1价,则NH4NO3中N的元素化合价为:c+(+1)×4=+1,则c=-3.d+(-2)×3=-1,d=+5;
(5)电解水时正极放出的气体为氧气,负极产生氢气,且氢气的体积为氧气的2倍.所以若产生5mL氧气,则负极产生10mL的氢气;
(6)元素的化合价是元素的原子在形成化合物时表现出来的一种性质,因此,在单质分子里,元素的化合价为0;
(7)地壳中含量最多的前五种元素是:氧、硅、铝、铁、钙,所以地壳中含量最多的元素是氧,含量最多的金属元素是铝,其符号分别为:O、Al;
故答案为:(1)2H2O2 2H2O+O2↑;(2)2KMnO4
2H2O+O2↑;(2)2KMnO4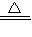 K2MnO4+MnO2+O2↑;(3)离子;阳离子;阴离子;Na+;Cl-;(4)+4;+7;-3;+5;
K2MnO4+MnO2+O2↑;(3)离子;阳离子;阴离子;Na+;Cl-;(4)+4;+7;-3;+5;
(5)10;(6)0;(7)O;Al;
点评:本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.
解答:解:(1)过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2
 2H2O+O2↑.
2H2O+O2↑.(2)高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式是2KMnO4
 K2MnO4+MnO2+O2↑.
K2MnO4+MnO2+O2↑.(3)原子得失电子后变成离子,带正电的离子叫阳离子,带负电的离子叫阴离子,NaCl是由Na+和Cl-构成的;
(4)根据在化合物中正负化合价代数和为零,可知:CO2中C元素的化合价为:a+(-2)×2=0,则a=+4;
KMnO4中Mn的元素化合价为:(+1)+b+(-2)×4=0,则b=+7;
铵根的化合价为+1价,硝酸根的化合价为-1价,则NH4NO3中N的元素化合价为:c+(+1)×4=+1,则c=-3.d+(-2)×3=-1,d=+5;
(5)电解水时正极放出的气体为氧气,负极产生氢气,且氢气的体积为氧气的2倍.所以若产生5mL氧气,则负极产生10mL的氢气;
(6)元素的化合价是元素的原子在形成化合物时表现出来的一种性质,因此,在单质分子里,元素的化合价为0;
(7)地壳中含量最多的前五种元素是:氧、硅、铝、铁、钙,所以地壳中含量最多的元素是氧,含量最多的金属元素是铝,其符号分别为:O、Al;
故答案为:(1)2H2O2
 2H2O+O2↑;(2)2KMnO4
2H2O+O2↑;(2)2KMnO4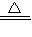 K2MnO4+MnO2+O2↑;(3)离子;阳离子;阴离子;Na+;Cl-;(4)+4;+7;-3;+5;
K2MnO4+MnO2+O2↑;(3)离子;阳离子;阴离子;Na+;Cl-;(4)+4;+7;-3;+5;(5)10;(6)0;(7)O;Al;
点评:本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

练习册系列答案
相关题目

