题目内容
(2006?山东)水是宝贵的资源,防止水污染的根本措施是消除污染源.已知某化工厂工业废水中含有硫酸.科技人员设计了边排放边中和硫酸的工艺来处理该工厂的废水,方案如下: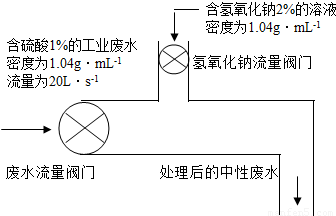
请你通过计算说明:要使该工厂废水达到排放要求,NaOH溶液的流量应为多少?
(计算结果精确到0.1)(相对原子质量:H-1 Na-23 S-32 O-16)
【答案】分析:根据图示可知,该工厂的废水处理发生反应的化学方程式为H2SO4+2NaOH═Na2SO4+2H2O,根据化学方程式,得出各物质之间的质量比,列出比例式,即可计算出NaOH溶液的流量.
解答:解:设NaOH溶液的流量为x.
H2SO4+2NaOH═Na2SO4+2H2O
98 80
20L/s×1000mL/L×1.04g/mL×1%,x×1000mL/L×1.04g/mL×2%
∴
解之得:x= ≈8.2L/s,
≈8.2L/s,
答:NaOH溶液的流量为8.2L/s.
点评:本题主要考查学生根据图示信息,得出化学方程式,再运用化学方程式,结合物理知识进行计算的能力.
解答:解:设NaOH溶液的流量为x.
H2SO4+2NaOH═Na2SO4+2H2O
98 80
20L/s×1000mL/L×1.04g/mL×1%,x×1000mL/L×1.04g/mL×2%
∴

解之得:x=
 ≈8.2L/s,
≈8.2L/s,答:NaOH溶液的流量为8.2L/s.
点评:本题主要考查学生根据图示信息,得出化学方程式,再运用化学方程式,结合物理知识进行计算的能力.

练习册系列答案
相关题目