题目内容
在宏观、微观和符号之间建立联系是化学学科的特点.
(1)用化学用语填空.
①2个硅原子 ;
② 的微粒符号 ;
的微粒符号 ;
③地壳中最多的金属元素和非金属元素组成的化合物 .
(2)A、B、C、D表示四种物质,其微观示意图如图1所示:
①从微观角度看,B图表示: .(填化学符号)
②从宠观角度看,图中表示混合物的是 .(填字母符号)
(3)在一定条件下,A和B能发生化学反应生成E和F,其微观示意图如图2所示:
①若F为空气中体积分数最大的气体,则该反应中生成的E和F的质量比 .
②若F为氧化物,且A和B的分子个数比为5:4,则该反应的化学方程式为 .

(1)用化学用语填空.
①2个硅原子
②
 的微粒符号
的微粒符号③地壳中最多的金属元素和非金属元素组成的化合物
(2)A、B、C、D表示四种物质,其微观示意图如图1所示:
①从微观角度看,B图表示:
②从宠观角度看,图中表示混合物的是
(3)在一定条件下,A和B能发生化学反应生成E和F,其微观示意图如图2所示:
①若F为空气中体积分数最大的气体,则该反应中生成的E和F的质量比
②若F为氧化物,且A和B的分子个数比为5:4,则该反应的化学方程式为

分析:(1)①原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.
②图中粒子,质子数=16,核外电子数=18,质子数<核外电子数,为硫离子.
③地壳中含量最多的金属元素是铝元素,含量最多的非金属元素是氧元素,组成的化合物为氧化铝
(2)同种分子构成的物质为纯净物,不同种分子构成的物质为混合物;再判断分子的构成,由同种原子构成的分子为单质的分子,由不同种原子构成的分子为化合物的分子.
(3)①F是空气中体积分数最大的气体(氮气),其反应物是氧气与氨气,产物是水与氮气,书写出化学反应方程式,对生成物的质量关系进行计算.
②根据质量守恒定律可知,F一定是氮的氧化物,用AB的分子个数比可确定其化学式,进而写出反应化学方程式.
②图中粒子,质子数=16,核外电子数=18,质子数<核外电子数,为硫离子.
③地壳中含量最多的金属元素是铝元素,含量最多的非金属元素是氧元素,组成的化合物为氧化铝
(2)同种分子构成的物质为纯净物,不同种分子构成的物质为混合物;再判断分子的构成,由同种原子构成的分子为单质的分子,由不同种原子构成的分子为化合物的分子.
(3)①F是空气中体积分数最大的气体(氮气),其反应物是氧气与氨气,产物是水与氮气,书写出化学反应方程式,对生成物的质量关系进行计算.
②根据质量守恒定律可知,F一定是氮的氧化物,用AB的分子个数比可确定其化学式,进而写出反应化学方程式.
解答:(1)①由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个硅原子表示为:2Si.
②图中粒子,质子数=16,核外电子数=18,质子数<核外电子数,为硫离子,其离子符号为:S2-.
③地壳中含量最多的金属元素是铝元素,含量最多的非金属元素是氧元素,组成的化合物为氧化铝,其化学式为:Al2O3.
(2)①从微观角度看,B图中三个分子构成相同,为同种物质的分子,1个该分子由1个氮原子和3个氢原子构成,其分子符号为:3NH3.
②C图中四个分子构成不同,为两种不同种物质的分子,一种分子由同种原子构成,为单质的分子;另一种分子由两种不同种的原子构成,为化合物的分子;该图所示物质为单质和化合物组成的混合物.
D图中五个分子构成不同,为三种不同种物质的分子,三种分子均由同种原子构成,均为单质的分子;该图所示物质为三种不同的单质组成的混合物.
(3)①F是氮气时,其反应物是氧气与氨气,产物是水与氮气,其方程式是3O2+4NH3
6H2O+2N2,则水与氮气的质量比为(6×18):(4×14)=27:14.
②由质量守恒定律可知,F一定是氮的氧化物,由A和B的分子个数比为5:4,可确定氮的氧化物为NO,则反应的化学方程式为:5O2+4NH3
6H2O+4NO.
(1)①2Si;②S2-;③Al2O3;
(2)①3NH3;②C、D;
(3)①27:14;②5O2+4NH3
6H2O+4NO.
②图中粒子,质子数=16,核外电子数=18,质子数<核外电子数,为硫离子,其离子符号为:S2-.
③地壳中含量最多的金属元素是铝元素,含量最多的非金属元素是氧元素,组成的化合物为氧化铝,其化学式为:Al2O3.
(2)①从微观角度看,B图中三个分子构成相同,为同种物质的分子,1个该分子由1个氮原子和3个氢原子构成,其分子符号为:3NH3.
②C图中四个分子构成不同,为两种不同种物质的分子,一种分子由同种原子构成,为单质的分子;另一种分子由两种不同种的原子构成,为化合物的分子;该图所示物质为单质和化合物组成的混合物.
D图中五个分子构成不同,为三种不同种物质的分子,三种分子均由同种原子构成,均为单质的分子;该图所示物质为三种不同的单质组成的混合物.
(3)①F是氮气时,其反应物是氧气与氨气,产物是水与氮气,其方程式是3O2+4NH3
| ||
②由质量守恒定律可知,F一定是氮的氧化物,由A和B的分子个数比为5:4,可确定氮的氧化物为NO,则反应的化学方程式为:5O2+4NH3
| ||
(1)①2Si;②S2-;③Al2O3;
(2)①3NH3;②C、D;
(3)①27:14;②5O2+4NH3
| ||
点评:本题难度不大,掌握常见化学用语(原子符号、化学式、离子符号等)的书写方法,学会通过微观示意图把宏观物质和微观粒子联系起来、从微观的角度分析物质的变化是正确解答本题的关键.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
在宏观、微观和符号之间建立联系是化学学科的特点.现有A、B、C、D四种物质,其微观示意图见下表.
(1)1个B物质分子中有 原子.
(2)上述物质中属于单质的是 ,属于有机物的是 .[填写化学式]
(3)C物质中两种元素的质量比为 .
(4)将一定质量的A、B、C、D四种物质放在一密闭的容器内中,在电火花作用下,发生充分反应,测得反应前后各物质的质量如下:
其中,a值为 ,该反应的化学方程式中A与D的化学计量数之比为 .
| 物质 | A | B | C | D |  --氢原子 --氢原子 --碳原子 --碳原子 --氧原子 --氧原子 |
| 微观示意图 |  |
 |
 |
 |
(2)上述物质中属于单质的是
(3)C物质中两种元素的质量比为
(4)将一定质量的A、B、C、D四种物质放在一密闭的容器内中,在电火花作用下,发生充分反应,测得反应前后各物质的质量如下:
| A | B | C | D | |
| 反应前质量/g | 25 | 1 | 10 | 74 |
| 反应后质量/g | 9 | 37 | a | 10 |

 ”、“
”、“ ”、“
”、“ ”分别表示A、B、C三种物质的分子,下图表示某化学反应前后反应物与生成物分子及其数目的变化.该化学方程式中A、B、C前的化学计量数之比为
”分别表示A、B、C三种物质的分子,下图表示某化学反应前后反应物与生成物分子及其数目的变化.该化学方程式中A、B、C前的化学计量数之比为

 表示A元素的原子,
表示A元素的原子, 表示B元素的原子.某反应前后的物质微观示意图如下.
表示B元素的原子.某反应前后的物质微观示意图如下.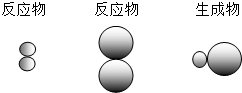
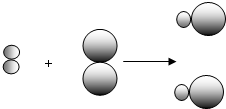 和
和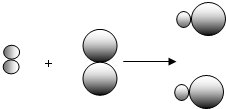 中的
中的 属于同种元素,这是因为这些原子含有相同的
属于同种元素,这是因为这些原子含有相同的 表示甲元素的原子,
表示甲元素的原子, 表示乙元素的原子.某反应前后的物质微观示意图如下.
表示乙元素的原子.某反应前后的物质微观示意图如下.


 属于同种元素,这是因为这些原子含有相同的
属于同种元素,这是因为这些原子含有相同的




