题目内容
【题目】碳酸氢钠、碳酸钠都是人们常用的膨松剂,对膨松剂的质量,国家有明确的要求。某兴趣小组在市场上发现一种食品膨松剂,其标签如下图所示。兴趣小组对该食品级膨松剂进行了检测,称取 4.00g 样品放入试管中,加热,试管中剩余物质的质量与加热时间的关系如下表所示(忽略其它杂质)。

已知:2NaHCO3![]() Na2CO3 + H2O +CO2↑ 。
Na2CO3 + H2O +CO2↑ 。
时间/min | 0 | 0.5 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 5.0 |
剩余物质量/g | 4.00 | 3.52 | 3.03 | 2.94 | 2.85 | 2.80 | 2.76 | 2.76 |
(1)反应最后产生的剩余物是_______。
(2)通过计算,判断该膨松剂中 NaHCO3 的质量分数是否符合上图的包装说明_______?(写出计算过程)
(3)若忽略其它杂质,将反应的剩余物放入_______mL 水中,充分溶解后,可得到 15.0% 的溶液。(精确到 0.1mL)
【答案】碳酸钠或Na2CO3 不符合包装说明 15.6mL
【解析】
(1)碳酸氢钠加热生成碳酸钠、水和二氧化碳,由于忽略其他杂质,所以反应最后剩余物质为碳酸钠;
(2)设该膨松剂中碳酸氢钠的质量为x:
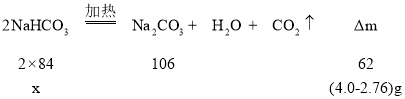
![]()
x=3.36g
该膨松剂中 NaHCO3 的质量分数是:![]()
该膨松剂中 NaHCO3 的质量分数不符合包装说明。
(3)设将反应的剩余物放入ymL水中,充分溶解后,可得到 15.0% 的溶液
![]()
解得y≈15.6mL

 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案【题目】全国人大和政协会议使用了一种含碳酸钙的“石头纸”:为测定其中碳酸钙的含量,课外活动小组的同学称取50g碎纸样品。分别在5只烧杯中进行了实验,实验数据见下表:(假设这种纸张中其它成分既不溶于水,也不与水反应):
烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
充分反应后生成 气体的质量/g | 0.88 | 1.76 | X | 3.52 | 3.52 |
(1)表中X的值为____________。
(2)求10g样品中碳酸钙的质量_________。
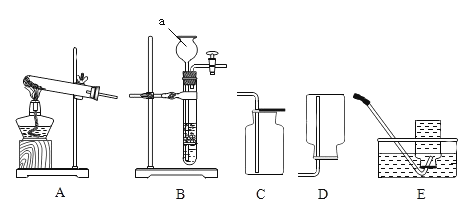
【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
A | B | C | D |
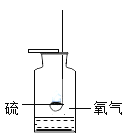
硫在氧气中燃烧
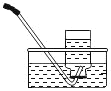
| 测定空气中氧气含量
| 铁丝在氧气中燃烧
| 排水法收集呼出的气体
|
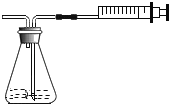
集气瓶中的水:吸收放出的热量 | 量筒中的水:通过水体积的变化得出O2体积 | 集气瓶中的水:冷却溅落融熔物,防止集气瓶炸裂 | 集气瓶中的水:水先将集气瓶内的空气排净,后便于观察呼出气体何时收集满 |
A.AB.BC.CD.D
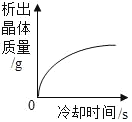
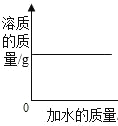
【题目】下列各图象不能正确反映其对应操作中各量变化关系的是( )
|
|
|
|
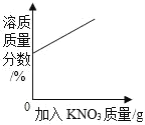
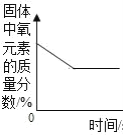
A某温度下热的硝酸钾饱和溶液逐渐冷却至室温 | B向一定量的氯化钠溶液中加水稀释 | C向一定量的硝酸钾不饱和溶液中加入硝酸钾 | D加热高锰酸钾固体 |
A.AB.BC.CD.D