题目内容
【题目】25g石灰石与146g稀盐酸恰好完全反应(杂质不参加反应)反应后残余物质量为162.2g.
(1)生成二氧化碳的质量为_____;
(2)石灰石中碳酸钙的质量分数。_____(写出计算过程)
【答案】8.8g 80%
【解析】
根据碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳;根据质量守恒定律,试管中质量的减少的质量即生成的二氧化碳质量,据此根据反应的化学方程式列式计算出生成的碳酸钙的质量,进而计算出石灰石中含碳酸钙的质量分数。
(1)由质量守恒定律,生成二氧化碳气体的质量为25g+146g-162.2g=8.8g;
(2)设原石灰石中CaCO3的质量为x,
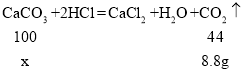
![]()
x=20g,
石灰石中CaCO3的质量分数为:![]() ×100%=80%;
×100%=80%;
答:(1)反应中生成的CO2质量为8.8g;
(2)石灰石中CaCO3的质量分数为80%。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目