题目内容
下列为实验室常用的实验装置,回答问题: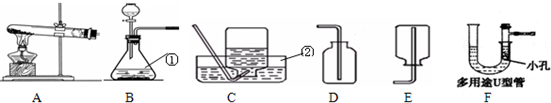
(1)写出带有标号仪器的名称:①______;②______.
(2)用A装置制取氧气的化学方程式是______.
(3)用B、E装置组合制取气体的化学方程式是______.F装置可代替B装置,若在反应进行中分别将两装置的橡胶管中部夹上止水夹,可能出现的现象是:B装置______;F装置______.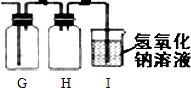
(4)硫化氢(H2S)是一种有毒的气体,能溶于水形成氢硫酸.实验室通常用块状固体硫化亚铁(FeS)和稀硫酸混合,在常温下发生反应制得硫化氢气体.某同学用右图
G、H、I装置组合来收集硫化氢气体,其中:
G装置说明硫化氢气体的密度比空气的______(填大或小);
H装置的作用是______;I装置的作用是______.
解:(1)本题为常见仪器的考查,识记住即可,分别为:①锥形瓶;②水槽.
(2)由A装置知,反应需要加热,反应物为固体,用加热高锰酸钾分解后生成锰酸钾、二氧化锰和氧气,故答案为:2KMnO4 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
(3)由B装置知,反应不需要加热,反应物为固体和液体,且收集气体用向下排空气法,所以用锌和稀硫酸反应制取氢气较适合,即反应方程式为:Zn+H2SO4═ZnSO4+H2↑;如将两装置的橡胶管中部夹上止水夹,生成的气体会让容器内气体的压强增大,达到一定程度,B装置中橡皮塞飞出,F装置由于气压增大会使右侧液面下降,固液分离,反应停止.故答案为:Zn+H2SO4═ZnSO4+H2↑;橡皮塞飞出;右侧液面下降,固液分离,反应停止
(4)根据反应物的状态和反应条件,制取硫化氢,可以选B作发生装置;硫化氢的密度比空气大,用E装置收集硫化氢;F装置的作用是G中倒吸的氢氧化钠溶液,防止氢氧化钠溶液进入E装置,因为硫化氢有毒,用氢氧化钠溶液吸收尾气,防止硫化氢污染空气.故答案为:大;防止I中的溶液倒吸进入G中; 吸收多余的H2S,防止污染空气.
分析:(1)根据常见仪器判断;
(2)根据装置选择制取氧气的方法;
(3)根据装置的原理选择反应物,根据收集的方法判断气体,根据气体的压强增大判断出现的后果;
(4)硫化亚铁(FeS)与稀硫酸在常温下反应生成硫化氢,可以选B作发生装置;但是硫化氢(H2S)是有毒气体,且密度比空气大,应用E装置收集,并用氢氧化钠溶液吸收尾气.
点评:本题主要考查常用气体的发生装置和收集装置的选取方法以及注意事项;并且要正确书写化学式和化学方程式;会利用题目中的信息处理问题.
(2)由A装置知,反应需要加热,反应物为固体,用加热高锰酸钾分解后生成锰酸钾、二氧化锰和氧气,故答案为:2KMnO4
 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑(3)由B装置知,反应不需要加热,反应物为固体和液体,且收集气体用向下排空气法,所以用锌和稀硫酸反应制取氢气较适合,即反应方程式为:Zn+H2SO4═ZnSO4+H2↑;如将两装置的橡胶管中部夹上止水夹,生成的气体会让容器内气体的压强增大,达到一定程度,B装置中橡皮塞飞出,F装置由于气压增大会使右侧液面下降,固液分离,反应停止.故答案为:Zn+H2SO4═ZnSO4+H2↑;橡皮塞飞出;右侧液面下降,固液分离,反应停止
(4)根据反应物的状态和反应条件,制取硫化氢,可以选B作发生装置;硫化氢的密度比空气大,用E装置收集硫化氢;F装置的作用是G中倒吸的氢氧化钠溶液,防止氢氧化钠溶液进入E装置,因为硫化氢有毒,用氢氧化钠溶液吸收尾气,防止硫化氢污染空气.故答案为:大;防止I中的溶液倒吸进入G中; 吸收多余的H2S,防止污染空气.
分析:(1)根据常见仪器判断;
(2)根据装置选择制取氧气的方法;
(3)根据装置的原理选择反应物,根据收集的方法判断气体,根据气体的压强增大判断出现的后果;
(4)硫化亚铁(FeS)与稀硫酸在常温下反应生成硫化氢,可以选B作发生装置;但是硫化氢(H2S)是有毒气体,且密度比空气大,应用E装置收集,并用氢氧化钠溶液吸收尾气.
点评:本题主要考查常用气体的发生装置和收集装置的选取方法以及注意事项;并且要正确书写化学式和化学方程式;会利用题目中的信息处理问题.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
氢氧化钠是化学实验室中的常用试剂,盛放NaOH溶液的试剂瓶瓶口常会出现白色粉末.化学兴趣小组的同学对这种白色粉末进行了实验探究.
他们依据所学的化学知识,对这种白色粉末的成分作了如下三种不同的猜想:
【提出猜想】
①甲同学认为可能是NaOH;
②乙同学认为可能是 ________;
③丙同学认为可能是NaOH和Na2CO3的混合物.
请将乙同学的猜想填写完整.为了验证猜想,他们进行了下面的实验:
【实验探究】
(1)甲同学取少量白色粉末溶于水,向所得溶液中滴加酚酞溶液,溶液变成红色.由此该同学认为白色粉末是NaOH.请判断他所得出的结论是否正确,并简述理由:________.
(2)乙同学为验证他的猜想,设计了下列实验,请将下列实验报告填写完整.
| 实 验 操 作 | 实 验 现 象 | 结 论 |
| 取少量白色粉末 滴加稀盐酸 | 有 ________生成 | 乙同学认为自己的猜想正确. 反应的方程式为: ________ |
(3)丙同学认为乙同学得出的结论不严密.为验证自己的猜想,该同学取少量白色粉末溶于水,向所得的溶液中滴加过量的BaCl2溶液,有白色沉淀产生,由此判断白色粉末中含有 ________;该同学继续向溶液中滴加 ________,证明了自己的猜想正确.
【问题讨论】如果实验室中没有BaCl2溶液,能否用Ba(OH)2溶液代替,并说明理由:________.
氢氧化钠是化学实验室中的常用试剂,盛放NaOH溶液的试剂瓶瓶口常会出现白色粉末.化学兴趣小组的同学对这种白色粉末进行了实验探究.
他们依据所学的化学知识,对这种白色粉末的成分作了如下三种不同的猜想:
【提出猜想】
①甲同学认为可能是NaOH;
②乙同学认为可能是 ;
③丙同学认为可能是NaOH和Na2CO3的混合物.
请将乙同学的猜想填写完整.为了验证猜想,他们进行了下面的实验:
【实验探究】
(1)甲同学取少量白色粉末溶于水,向所得溶液中滴加酚酞溶液,溶液变成红色.由此该同学认为白色粉末是NaOH.请判断他所得出的结论是否正确,并简述理由:.
(2)乙同学为验证他的猜想,设计了下列实验,请将下列实验报告填写完整.
(3)丙同学认为乙同学得出的结论不严密.为验证自己的猜想,该同学取少量白色粉末溶于水,向所得的溶液中滴加过量的BaCl2溶液,有白色沉淀产生,由此判断白色粉末中含有 ;该同学继续向溶液中滴加 ,证明了自己的猜想正确.
【问题讨论】如果实验室中没有BaCl2溶液,能否用Ba(OH)2溶液代替,并说明理由:.
他们依据所学的化学知识,对这种白色粉末的成分作了如下三种不同的猜想:
【提出猜想】
①甲同学认为可能是NaOH;
②乙同学认为可能是 ;
③丙同学认为可能是NaOH和Na2CO3的混合物.
请将乙同学的猜想填写完整.为了验证猜想,他们进行了下面的实验:
【实验探究】
(1)甲同学取少量白色粉末溶于水,向所得溶液中滴加酚酞溶液,溶液变成红色.由此该同学认为白色粉末是NaOH.请判断他所得出的结论是否正确,并简述理由:.
(2)乙同学为验证他的猜想,设计了下列实验,请将下列实验报告填写完整.
| 实 验 操 作 | 实 验 现 象 | 结 论 |
| 取少量白色粉末 滴加稀盐酸 | 有 生成 | 乙同学认为自己的猜想正确. 反应的方程式为: |
(3)丙同学认为乙同学得出的结论不严密.为验证自己的猜想,该同学取少量白色粉末溶于水,向所得的溶液中滴加过量的BaCl2溶液,有白色沉淀产生,由此判断白色粉末中含有 ;该同学继续向溶液中滴加 ,证明了自己的猜想正确.
【问题讨论】如果实验室中没有BaCl2溶液,能否用Ba(OH)2溶液代替,并说明理由:.
 如图是常用的实 验装置图,根据所学知识回答下列问题:
如图是常用的实 验装置图,根据所学知识回答下列问题: