题目内容
木糖醇是一种理想的蔗糖替代品,适合糖尿病患者食用.
(1)木糖醇的化学式为C5H12O5,它是由________种元素组成的.木糖醇和蔗糖的溶解度曲线如图甲,据图回答:
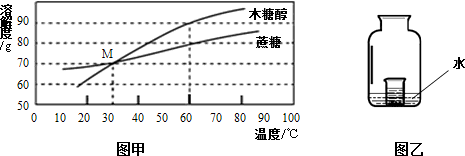
(2)①图甲中M点表示的含义是________.
②60℃时,向l00g水中加入80g木糖醇,充分溶解后,所得的溶液是________溶液(选填“饱和”或“不饱和”),
③若将30℃时蔗糖的不饱和溶液转变成饱和溶液,可采用的一种方法是________;若将30℃时340g 20%的蔗糖溶液浓缩成40%的溶液,应蒸发________g 水.
④将30℃时,将木糖醇和蔗糖分别形成的饱和溶液(固体全溶解)温度升高到60℃时,两种溶液中溶质的质量分数:木糖醇________蔗糖(选填“大于”、“小于”或“相等”).
⑤如图乙所示,在常温下,将蔗糖和水加到小烧杯中,充分溶解后仍然有少量的蔗糖未溶解,然后把小烧杯放到盛有水的大广口瓶中.若将少量的下列物质分别小心地加入到大广口瓶中,不断搅拌,能够使小烧杯中的蔗糖溶液溶质的质量分数增大的是________(填序号).
a.浓硫酸 b.硝酸铵 c.氢氧化钠 d.冰.
解:(1)木糖醇的化学式为C5H12O5,可知木糖醇含有碳、氢、氧三种元素,故(1)答案:三
(2)①由题中溶解度曲线可知M点是木糖醇和蔗糖溶解度的交点,表示30℃时木糖醇和蔗糖的溶解度相同,故①答案:30℃时木糖醇和蔗糖的溶解度都为70g
②在一定的温度下,某固体物质在100克溶剂里达到饱和溶液时所能溶解的质量,就是该种物质的溶解度.又因为60℃时木糖醇的溶解度为90g,故60℃时,向l00g水中加入80g木糖醇形成的溶液为不饱和溶液,故②答案:不饱和
③蔗糖的溶解度随温度的升高而增大,不饱和溶液转化为饱和溶液可采用降低温度或加入蔗糖或蒸发溶剂水的方法;若将30℃时340g 20%的蔗糖溶液浓缩成40%的溶液,若无溶质析出蒸发掉170g溶剂水溶质质量分数就变为40%.因为30℃时340g 20%的蔗糖溶液中溶质的质量为68g,溶剂水为340g-68g=272g,该温度下蔗糖的溶解度为70g,所以蒸发掉170g水,溶剂水还有102g,100g水中在该温度下溶解70g蔗糖才达到饱和,故68g蔗糖溶于102g水中形成该温度下的不饱和溶液.故③答案:降低温度或加入蔗糖或蒸发溶剂 170
④将30℃时,木糖醇和蔗糖分别形成的饱和溶液(固体全溶解)温度升高到60℃时,两种物质的溶解度都增大了,不会有固体析出;30℃时木糖醇和蔗糖的溶解度都为70g,故30℃时两种物质的饱和溶液溶质质量分数相等,升高温度到60℃时两种物质的溶解度都增大了,不会有固体析出,两种溶液溶质质量分数不变仍然相等,故④答案:相等.
浓硫酸、氢氧化钠溶于水放出大量的热,硝酸铵溶于水吸收热量,冰融化也会吸收热量;蔗糖的溶解度随温度的升高而增大,在常温下,将蔗糖和水加到小烧杯中,充分溶解后仍然有少量的蔗糖未溶解,升高温度可使未溶解的蔗糖溶解,故⑤答案:ac
分析:(1)运用化学式的意义解答木糖醇的元素组成.
(2)①运用溶解度曲线上某一点的意义解答.
②运用在一定的温度下,某固体物质在100克溶剂里达到饱和溶液时所能溶解的质量,就是该种物质的溶解度;再结合60℃时木糖醇的溶解度为90g解答.
③运用不饱和溶液和饱和溶液相互转化的方法和溶质质量分数的公式解答.
④运用该温度下两种物质的溶解度和溶质质量分数的计算公式解答
⑤运用温度升高该物质的溶解度增大和浓硫酸、氢氧化钠溶于水都放热解答.
点评:本题考查了从溶解度曲线图上读取信息、分析及获取信息的能力.从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同.
(2)①由题中溶解度曲线可知M点是木糖醇和蔗糖溶解度的交点,表示30℃时木糖醇和蔗糖的溶解度相同,故①答案:30℃时木糖醇和蔗糖的溶解度都为70g
②在一定的温度下,某固体物质在100克溶剂里达到饱和溶液时所能溶解的质量,就是该种物质的溶解度.又因为60℃时木糖醇的溶解度为90g,故60℃时,向l00g水中加入80g木糖醇形成的溶液为不饱和溶液,故②答案:不饱和
③蔗糖的溶解度随温度的升高而增大,不饱和溶液转化为饱和溶液可采用降低温度或加入蔗糖或蒸发溶剂水的方法;若将30℃时340g 20%的蔗糖溶液浓缩成40%的溶液,若无溶质析出蒸发掉170g溶剂水溶质质量分数就变为40%.因为30℃时340g 20%的蔗糖溶液中溶质的质量为68g,溶剂水为340g-68g=272g,该温度下蔗糖的溶解度为70g,所以蒸发掉170g水,溶剂水还有102g,100g水中在该温度下溶解70g蔗糖才达到饱和,故68g蔗糖溶于102g水中形成该温度下的不饱和溶液.故③答案:降低温度或加入蔗糖或蒸发溶剂 170
④将30℃时,木糖醇和蔗糖分别形成的饱和溶液(固体全溶解)温度升高到60℃时,两种物质的溶解度都增大了,不会有固体析出;30℃时木糖醇和蔗糖的溶解度都为70g,故30℃时两种物质的饱和溶液溶质质量分数相等,升高温度到60℃时两种物质的溶解度都增大了,不会有固体析出,两种溶液溶质质量分数不变仍然相等,故④答案:相等.
浓硫酸、氢氧化钠溶于水放出大量的热,硝酸铵溶于水吸收热量,冰融化也会吸收热量;蔗糖的溶解度随温度的升高而增大,在常温下,将蔗糖和水加到小烧杯中,充分溶解后仍然有少量的蔗糖未溶解,升高温度可使未溶解的蔗糖溶解,故⑤答案:ac
分析:(1)运用化学式的意义解答木糖醇的元素组成.
(2)①运用溶解度曲线上某一点的意义解答.
②运用在一定的温度下,某固体物质在100克溶剂里达到饱和溶液时所能溶解的质量,就是该种物质的溶解度;再结合60℃时木糖醇的溶解度为90g解答.
③运用不饱和溶液和饱和溶液相互转化的方法和溶质质量分数的公式解答.
④运用该温度下两种物质的溶解度和溶质质量分数的计算公式解答
⑤运用温度升高该物质的溶解度增大和浓硫酸、氢氧化钠溶于水都放热解答.
点评:本题考查了从溶解度曲线图上读取信息、分析及获取信息的能力.从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
下列对一些事实解释不正确的是
| 事实 | 解释 | |
| A | 二氧化碳无毒,而一氧化碳有毒 | 物质组成元素不同,分子结构也不同 |
| B | 0℃时水结成冰,而海水在-1.9℃才会结冰 | 海水中溶解的盐,使其凝固点降低 |
| C | 蒸发水和电解水是两种不同类型的变化 | 变化中,前者没有新物质生成,后者有新物质生成 |
| D | KMnO4溶液和K2SO4溶液的颜色不同 | 两种溶液中的阴离子不同 |
- A.二氧化碳无毒,而一氧化碳有毒 物质组成元素不同,分子结构也不同
- B.0℃时水结成冰,而海水在-1.9℃才会结冰 海水中溶解的盐,使其凝固点降低
- C.蒸发水和电解水是两种不同类型的变化 变化中,前者没有新物质生成,后者有新物质生成
- D.KMnO4溶液和K2SO4溶液的颜色不同 两种溶液中的阴离子不同



