题目内容
下列计算结果或算式正确的是( )A.Ca(OH)2的相对分子质量为40+16+1×2=58
B.SO2中硫元素与氧元素的质量比为1:1
C.C2H5OH中碳、氢、氧原子个数比为2:5:1
D.NH4NO3中氮元素的质量分数为
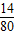 ×100%
×100%
【答案】分析:A、根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
C、根据乙醇分子的构成进行分析判断.
D、根据化合物中元素的质量分数= ×100%,进行分析判断.
×100%,进行分析判断.
解答:解:A、Ca(OH)2的相对分子质量为:40+(16+1)×2=74,故选项说法错误.
B、SO2中硫元素与氧元素的质量比为32:(1×6)=1:1,故选项说法正确.
C、1个乙醇分子是由2个碳原子、6个氢原子和1个氧原子构成的,则C2H5OH中碳、氢、氧原子个数比为2:6:1,故选项说法错误.
D、NH4NO3中氮元素的质量分数为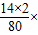 100%,故选项说法错误.
100%,故选项说法错误.
故选B.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
C、根据乙醇分子的构成进行分析判断.
D、根据化合物中元素的质量分数=
 ×100%,进行分析判断.
×100%,进行分析判断.解答:解:A、Ca(OH)2的相对分子质量为:40+(16+1)×2=74,故选项说法错误.
B、SO2中硫元素与氧元素的质量比为32:(1×6)=1:1,故选项说法正确.
C、1个乙醇分子是由2个碳原子、6个氢原子和1个氧原子构成的,则C2H5OH中碳、氢、氧原子个数比为2:6:1,故选项说法错误.
D、NH4NO3中氮元素的质量分数为
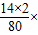 100%,故选项说法错误.
100%,故选项说法错误.故选B.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
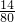 ×100%
×100%