题目内容
(2009?高淳县二模)为了做生石灰与水反应制熟石灰的实验,老师请同事从石灰窑中取出一些白色固体,现带来几小块,我们一起来探究一下.| 探究目的 | 探究步骤 | 现象 |
| 证明固体是否存在CaO | (1)取少量白色固体于烧杯,加入少量水后过滤,向滤液中滴加酚酞试液. | __________ |
| 证明固体是否存在CaCO3 | (2)向(1)所得滤渣滴加_____溶液 | 没有气体冒出 |
【答案】分析:欲正确解答本题,须知高温煅烧石灰石的化学方程式,根据化学方程式进行计算,就可得出正确结论.
解答:解:(1)高温煅烧石灰石的化学方程式为:CaCO3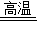 CaO+CO2↑;
CaO+CO2↑;
因为是从石灰窑中取出一些白色固体,故可能是氧化钙和碳酸钙的混合物.
(2)根据化学方程式CaO+2HCl=CaCl2+H2O,Ca(OH)2+2HCl=CaCl2+2H2O可知,等质量的CaO和Ca(OH)2与盐酸完全反应,Ca(OH)2所消耗的盐酸质量比CaO消耗的盐酸的质量少.故如果M2<M1,则说明白色固体中存在氢氧化钙.
故答案为:逐滴加入C%的稀盐酸并震荡,直到固体恰好全部消失,共消耗稀盐酸M2g,M2<M1.
点评:本题主要考查学生正确书写化学方程式的能力,以及运用化学方程式进行计算的能力.
解答:解:(1)高温煅烧石灰石的化学方程式为:CaCO3
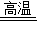 CaO+CO2↑;
CaO+CO2↑;因为是从石灰窑中取出一些白色固体,故可能是氧化钙和碳酸钙的混合物.
(2)根据化学方程式CaO+2HCl=CaCl2+H2O,Ca(OH)2+2HCl=CaCl2+2H2O可知,等质量的CaO和Ca(OH)2与盐酸完全反应,Ca(OH)2所消耗的盐酸质量比CaO消耗的盐酸的质量少.故如果M2<M1,则说明白色固体中存在氢氧化钙.
故答案为:逐滴加入C%的稀盐酸并震荡,直到固体恰好全部消失,共消耗稀盐酸M2g,M2<M1.
点评:本题主要考查学生正确书写化学方程式的能力,以及运用化学方程式进行计算的能力.

练习册系列答案
相关题目

