题目内容
【题目】某氢氧化钠样品中混有氯化钠,为测定样品中氢氧化钠的质量分数,称取5g样品,加入27g水完全溶解后,缓慢加入稀盐酸,同时测定溶液的pH。当pH=7时,刚好用去10%的稀盐酸36.5g。试计算:
(1)将100g质量分数为38%的浓盐酸稀释成10%的稀盐酸,需加水的质量为_____g。
(2)样品中氢氧化钠的质量_____。
(3)反应后所得溶液中溶质的质量分数_____。
【答案】280 4g 10%
【解析】
(1)稀释前后溶质的质量不变;
(2)根据化学方程式利用氯化氢的质量进行计算;
(3)根据化学方程式利用氯化氢的质量计算出生成氯化钠的质量,根据溶质质量分数计算公式进行计算。
(1)稀释前后溶质的质量不变,设加水的质量为x,100g×38%=(100g+x)×10% ,x=280g;
(2)所有36.5g10%的稀盐酸中溶质的质量为:36.5g×10%=3.65g
设氢氧化钠的质量为y,生成氯化钠的质量为z,
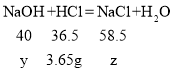
![]() y=4g,
y=4g,
![]() z=5.85g;
z=5.85g;
(3)反应后所得溶液中溶质的质量分数:![]() ×100%=10%。
×100%=10%。
答:(1)将100g质量分数为38%的浓盐酸稀释成10%的稀盐酸,需加水的质量为280g;(2)样品中氢氧化钠的质量4g;(3)反应后所得溶液中溶质的质量分数为10%。

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目