题目内容
【题目】下图所示的甲、乙两装置都可以用来进行木炭还原氧化铜的实验,小刚同学选用甲装置来进行实验:
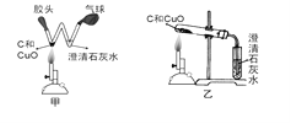
(1)在实验过程中,W形管的左边能观察到的现象是___________________________。
(2)实验时,小刚先观察到W形管右边的澄清石灰水变浑浊,发生反应的化学方程式为____________。
(3)实验过程中,小刚发现W管右端的气球鼓起来了,实验结束冷却到室温后,气球依然鼓着,他经过探究发现气球中的气体是CO2和CO的混合物。小刚对CO产生的原因进行了猜测:可能是木炭和氧化铜在高温条件下直接发生反应产生CO,这个反应的化学方程式为______________________;也可能是反应C+2CuO![]() 2Cu+CO2↑产生的CO2和多余的木炭发生了新的化学反应,产生了CO。这个实验说明,相同的反应物发生化学变化时,因为________________不同,可能得到不同的生成物。
2Cu+CO2↑产生的CO2和多余的木炭发生了新的化学反应,产生了CO。这个实验说明,相同的反应物发生化学变化时,因为________________不同,可能得到不同的生成物。
(4)甲乙两种装置相比,甲装置的优点之一是______________________________。
【答案】 固体由黑色变成红色 CO2+ Ca(OH)2=CaCO3↓+H2O C +CuO![]() Cu + CO↑ 反应物的量不 将尾气收集,避免尾气中的一氧化碳排放到空气中,污染空气。
Cu + CO↑ 反应物的量不 将尾气收集,避免尾气中的一氧化碳排放到空气中,污染空气。
【解析】书写化学方程式的步骤一般有四步:1.根据实验事实,在式子的左、右两边分别写出反应物和生成物的化学式,并在式子的左、右两边之间画一条短线;当反应物或生成物有多种时,中间用加号(即“+”)连接起来。2.配平化学方程式,并检查后,将刚才画的短线改写成等号(表示式子左、右两边每一种元素原子的总数相等)。3.标明化学反应发生的条件(因为化学反应只有在一定的条件下才能发生);如点燃、加热(常用“△”号表示)、催化剂、通电等。并且,一般都写在等号的上面,若有两个条件,等号上面写一个下面写一个。4.注明生成物中气体或固体的状态符号(即“↑”、“↓”);一般标注在气体或固体生成物的化学式的右边。但是,如果反应物和生成物中都有气体或固体时,其状态符号就不用标注了。(1)在实验过程中,W形管的左边发生的反应是碳和氧化铜在高温条件下生成铜和二氧化碳,能观察到的现象是固体由黑色变成红色;(2)实验时, W形管右边的澄清石灰水变浑浊,因为生成的二氧化碳和石灰水中的溶质氢氧化钙反应生成碳酸钙沉淀和水,发生反应的化学方程式为CO2 + Ca(OH)2 == CaCO3↓+ H2O;(3)木炭和氧化铜在高温条件下直接发生反应产生CO,这个反应的化学方程式为C + CuO高温 Cu + CO↑;也可能是反应C+2CuO![]() 2Cu+CO2↑,产生的CO2和多余的木炭发生了新的化学反应,产生了CO。这个实验说明,相同的反应物发生化学变化时,因为反应物的量不同,可能得到不同的生成物;(4)甲乙两种装置相比,甲装置的优点之一是将尾气收集,避免尾气中的一氧化碳排放到空气中,污染空气。
2Cu+CO2↑,产生的CO2和多余的木炭发生了新的化学反应,产生了CO。这个实验说明,相同的反应物发生化学变化时,因为反应物的量不同,可能得到不同的生成物;(4)甲乙两种装置相比,甲装置的优点之一是将尾气收集,避免尾气中的一氧化碳排放到空气中,污染空气。

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案



