题目内容
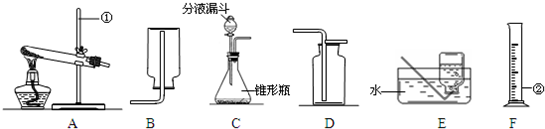
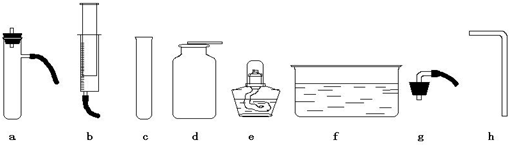
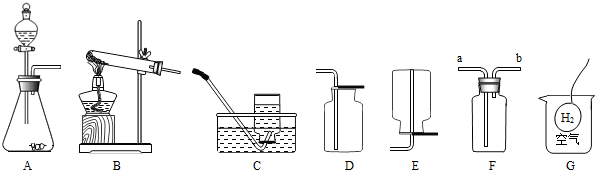
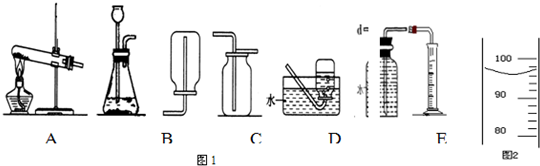
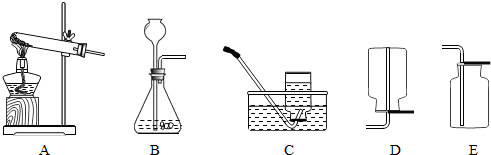
下图是实验室常用的实验仪器与装置.依据题目要求回答下列问题:

(1)写出标号仪器的名称:①______;②______.
(2)采用分解过氧化氢溶液与二氧化锰的混合物的方法制取氧气有许多优点,如______(填序号).
①产物无污染 ②不需加热 ③需加热 ④生成物只有氧气.
(3)为确定某集气瓶最多可收集氧气的体积,请设计一个简便的测量方法(仪器用品等任选):______.
(4)甲同学用分解过氧化氢溶液的方法制取并收集氧气,应分别选择装置______(填字母);除过氧化氢溶液外,通常还需要一种药品是______(填化学式),其作用是______,加入药品前应注意检查装置的______性.
解:(1)仪器名称为:试管,集气瓶;(2)双氧水制氧气不需加热,生成物是水和氧气,无污染;
(3)要测量集气瓶中氧气的体积,只需测一瓶水的体积即可;
(4)过氧化氢制取氧气发生装置要选择固液常温型装置,氧气不易溶于水,密度比空气大,可用排水法和向上排空气法收集;过氧化氢常温下也能分解,但反应速度很慢,加入二氧化锰能加快双氧水的分解速度,起催化作用;为防止装置漏气,收集不到气体,在制取气体前要先检验装置的气密性.
故答案为:(1)试管,集气瓶;(2)①②;(3)集气瓶装满水倒入量筒内读出体积即为瓶内氧气的体积
(4)AD(或E)或BD(或E);MnO2催化作用;气密
分析:双氧水制氧气不需加热,生成物是水和氧气,无污染;测量气体体积只能等量转化成液体才能测量其体积;二氧化锰是双氧水分解的催化剂.
点评:量筒只能测量液体的体积,要测量气体体积可将气体等量转化成液体进行测量.
(3)要测量集气瓶中氧气的体积,只需测一瓶水的体积即可;
(4)过氧化氢制取氧气发生装置要选择固液常温型装置,氧气不易溶于水,密度比空气大,可用排水法和向上排空气法收集;过氧化氢常温下也能分解,但反应速度很慢,加入二氧化锰能加快双氧水的分解速度,起催化作用;为防止装置漏气,收集不到气体,在制取气体前要先检验装置的气密性.
故答案为:(1)试管,集气瓶;(2)①②;(3)集气瓶装满水倒入量筒内读出体积即为瓶内氧气的体积
(4)AD(或E)或BD(或E);MnO2催化作用;气密
分析:双氧水制氧气不需加热,生成物是水和氧气,无污染;测量气体体积只能等量转化成液体才能测量其体积;二氧化锰是双氧水分解的催化剂.
点评:量筒只能测量液体的体积,要测量气体体积可将气体等量转化成液体进行测量.

练习册系列答案
相关题目
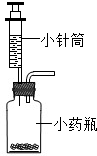 (3)实验室制取二氧化碳的化学方程式为
(3)实验室制取二氧化碳的化学方程式为