题目内容
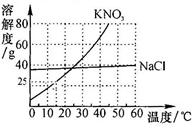
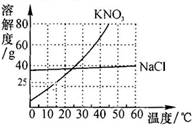
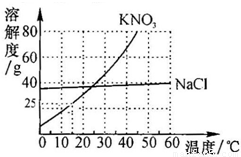
实验小组帮助老师配置KNO3的饱和溶液,以备全班实验使用.此实验室温度为15℃,老师提供的药品是含有少量NaCl的KNO3固体.(1)查阅了两种物质的溶解度曲线,如图所示.KNO3中混有少量NaCl的提纯方法是______,用此法获得了足量的KNO3固体.
(2)配置100gKNO3饱和溶液的过程如下:
①计算;
②称量:准确称量KNO3固体______g;
称取过程中,发现指针已偏向分度盘左侧,接下来的操作是______;
③量取:用______(填“50ml”、“100ml”或“500ml”) 量筒量取蒸馏水;
④溶解:将KNO3固体和水分别加入大烧杯中,搅拌使固体完全溶解.
(3)若小组同学最后配得的KNO3溶液溶质的质量分数偏小,可能的原因是______
①用量筒量取水时俯视读数;
②配制溶液时烧杯用少量蒸馏水润洗;
③在托盘天平的左盘放砝码,右盘放KNO3称量;
④天平称量时,指针偏向左盘药品⑤将固体倒入烧杯时有部分洒出.
A.①④B.②④⑤C.②③⑤D.②⑤

【答案】分析:(1)根据提纯物质的溶解度与温度的关系考虑;(2)②根据15℃硝酸钾的溶解度为25g计算出100g饱和硝酸钾溶液中溶质质量;发现指针已偏向分度盘左侧说明硝酸钾多了,应该减少硝酸钾;③配制100gKNO3饱和溶液,所以水的体积小于100mL;(3)配得的KNO3溶液溶质的质量分数偏小,要从两个方面分析:溶质称少了,溶剂量多了.
解答:解;(1)KNO3中混有少量NaCl,提纯的是硝酸钾,因为硝酸钾的溶解度随温度的变化比较大,所以用冷却热饱和溶液的方法,或降温结晶;
(2)②15℃硝酸钾的溶解度为25g,设100g饱和硝酸钾溶液中含溶质质量为X则: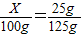 解得X=20g;发现指针已偏向分度盘左侧说明硝酸钾多了,应该减少硝酸钾;
解得X=20g;发现指针已偏向分度盘左侧说明硝酸钾多了,应该减少硝酸钾;
③配制100gKNO3饱和溶液,所以水的体积小于100mL,并且选择与所量液体最接近的;
(3)用量筒量取水时俯视读数,量取到的液体水偏少,即配得的质量分数会偏大;配制溶液时烧杯用少量蒸馏水润洗,说明水多了,配得的质量分数会偏小;在托盘天平的左盘放砝码,右盘放KNO3称量,称得的质量偏小,所以配得的质量分数会偏小;天平称量时,指针偏向左盘药品,说明药品称多了,配得的质量分数会偏大;将固体倒入烧杯时有部分洒出,会导致溶质偏小,配得的质量分数会偏小.
故答案为:(1)降温结晶;(2)②20;减少硝酸钾;③100ml;(3)C.
点评:解答本题容易出错的地方是溶质质量分数偏小的原因:要从两个方面分析:溶质称少了,溶剂量多了.
解答:解;(1)KNO3中混有少量NaCl,提纯的是硝酸钾,因为硝酸钾的溶解度随温度的变化比较大,所以用冷却热饱和溶液的方法,或降温结晶;
(2)②15℃硝酸钾的溶解度为25g,设100g饱和硝酸钾溶液中含溶质质量为X则:
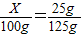 解得X=20g;发现指针已偏向分度盘左侧说明硝酸钾多了,应该减少硝酸钾;
解得X=20g;发现指针已偏向分度盘左侧说明硝酸钾多了,应该减少硝酸钾;③配制100gKNO3饱和溶液,所以水的体积小于100mL,并且选择与所量液体最接近的;
(3)用量筒量取水时俯视读数,量取到的液体水偏少,即配得的质量分数会偏大;配制溶液时烧杯用少量蒸馏水润洗,说明水多了,配得的质量分数会偏小;在托盘天平的左盘放砝码,右盘放KNO3称量,称得的质量偏小,所以配得的质量分数会偏小;天平称量时,指针偏向左盘药品,说明药品称多了,配得的质量分数会偏大;将固体倒入烧杯时有部分洒出,会导致溶质偏小,配得的质量分数会偏小.
故答案为:(1)降温结晶;(2)②20;减少硝酸钾;③100ml;(3)C.
点评:解答本题容易出错的地方是溶质质量分数偏小的原因:要从两个方面分析:溶质称少了,溶剂量多了.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 实验小组帮助老师配置KNO3的饱和溶液,以备全班实验使用.此实验室温度为15℃,老师提供的药品是含有少量NaCl的KNO3固体.
实验小组帮助老师配置KNO3的饱和溶液,以备全班实验使用.此实验室温度为15℃,老师提供的药品是含有少量NaCl的KNO3固体.