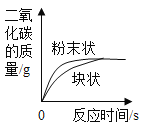
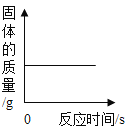
题目内容
【题目】(1)实验室有带橡胶管的玻璃导管和下列仪器、装置可供选择,请填空:
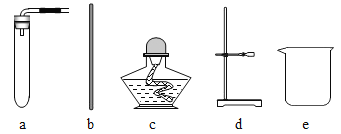
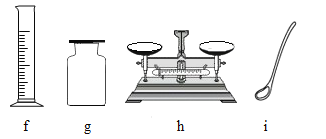
①用过氧化氢和二氧化锰制取并收集O2 ,所用仪器或装置有__________。(填序号)。
②用氯酸钾和二氧化锰制取O2,反应的化学方程式是_____________。
③要配制400g5%的NaOH溶液,所需NaOH固体的质量为______g,若称取NaOH固体所用小烧杯的质量为18.5 g,托盘天平的标尺最大刻度为5 g,砝码有5g、10g 、20 g、50 g几种规格,则称量时放在天平右盘的砝码质量为_________g;配制过程所需仪器除e、f、h和小烧杯、试剂瓶外,还需要_________(填仪器名称)。
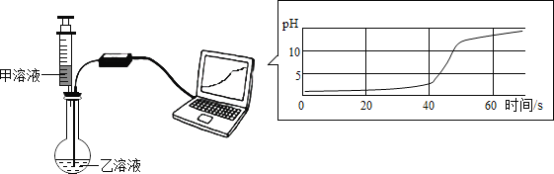
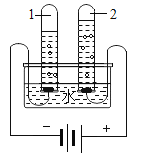
(2)某兴趣小组同学将CO2分别通入澄清石灰水和氢氧化钠溶液中,观察到前者变浑浊,后者无明显现象。为探究CO2和NaOH是否发生了化学反应,王强设计了如图所示的A、B实验,验证CO2与NaOH溶液发生了化学反应。实验现象为;A中试管内液面上升;B中气球胀大。
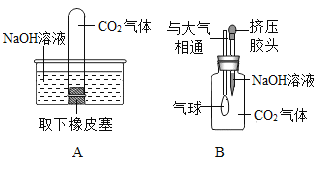
①王强认为上述实验是可行的,其共同原理是_________。
②李莉提出质疑,她认为上述实验不严谨,其理由是__________。要得到科学严谨的结论,仍利用该装置,补做的对比实验是____________
③杨红通过检验生成物:向B实验后的溶液中加入_____,观察到__________现象,从而也证明CO2与NaOH发生了反应。
④你认为两实验中存在安全隐患的是_________(填代号) ,理由是__________。
【答案】a、d、g、i 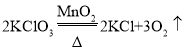 20g 35 胶头滴管、玻璃棒、药匙 氢氧化钠溶液与二氧化碳反应,使容器内气压降低 CO2能溶于水,也能使容器内气压降低 将氢氧化钠溶液换成等体积的水 足量的稀盐酸 有气泡产生 A 氢氧化钠溶液有腐蚀性,取下橡皮塞时,存在安全隐患
20g 35 胶头滴管、玻璃棒、药匙 氢氧化钠溶液与二氧化碳反应,使容器内气压降低 CO2能溶于水,也能使容器内气压降低 将氢氧化钠溶液换成等体积的水 足量的稀盐酸 有气泡产生 A 氢氧化钠溶液有腐蚀性,取下橡皮塞时,存在安全隐患
【解析】
(1)①用过氧化氢和二氧化锰制取氧气,属于“固液常温型”制气体,据此选择仪器;
②氯酸钾在加热的条件和二氧化锰的催化作用下,生成氯化钾和氧气;
③根据氢氧化钠的性质、溶质质量计算公式作答;
(2)二氧化碳与氢氧化钠反应生成碳酸钠和水,据此分析作答。
(1)①根据分析,选择装置a作为反应装置、d固定试管、g收集氧气、i取固体药品,故填:a、d、g、i;
②根据分析,故填: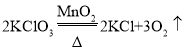 ;
;
③氢氧化钠有强烈的腐蚀性,要放在小烧杯中称量,依据溶质的质量=溶液的质量×溶质的质量分数,可以求出溶质的质量是400g×5%=20g,与烧杯的总质量是38.5g,结合题意,所加砝码的质量是35g,配制溶液需仪器除了题目提供的仪器以外,还需要胶头滴管、玻璃棒和药匙,
故填:20g;35;胶头滴管、玻璃棒、药匙;
(2)①氢氧化钠溶液吸收了二氧化碳后,使集气瓶和试管中的压强减小,在外界大气压的作用下A中试管的液面上升,B中气球胀大,故填:氢氧化钠溶液与二氧化碳反应,使容器内气压降低;
②二氧化碳不但能与氢氧化钠反应,还能与水反应,试管中的压强一样能减小把A中的氢氧化钠溶液换成水再做此实验仍能成立,故填:CO2能溶于水,也能使容器内气压降低;将氢氧化钠溶液换成等体积的水;
③实验后的溶液为碳酸钠溶液,加入足量的盐酸溶液有气泡产生,从而证明CO2与NaOH发生了反应,故填:稀盐酸;有气泡产生;
④两实验中A的溶液是氢氧化钠溶液有腐蚀性,取下橡皮塞时,存在安全隐患,故填:A;氢氧化钠溶液有腐蚀性。

 智慧小复习系列答案
智慧小复习系列答案