题目内容
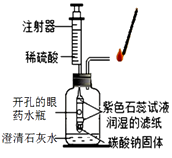
【题目】如图是电解水实验装置。
(1)在实验过程中,试管a产生的气体是 , 如果试管a中气体的体积为10mL,则试管b中气体的体积约为。写出水在通电条件下反应的表达式 , 该反应的基本类型是。
(2)试管a中气体,将使用燃烧着的木条还是带火星的木条进行检验? , 观察到的现象是。
(3)分析水分子分解示意图:在直流电的作用下,水分子分解成 , 每两个氧原子结合成 , 每两个氢原子结合成。由此可知化学变化中最小粒子是(填“分子”或“原子”)。
【答案】
(1)氢气,5毫升,![]() ,分解反应
,分解反应
(2)燃烧着的木条,气体燃烧、发出淡蓝色火焰
(3)氢原子、氧原子,一个氧分子,一个氢分子,原子
【解析】解:(1)水在通电条件下分解生成氢气和氧气,正极生成氧气,负极生成氢气,正负两极气体体积比为1:2,反应方程式为:![]() ,属于分解反应;(2)氢气常用燃着的木条检验,现象是气体燃烧,有淡蓝色的火焰;(3)水分解的实质是:每个水分子分成两个氢原子和一个氧原子,然后每两个氢原子结合成一个氢分子;每两个氧原子结合成一个氧分子。
,属于分解反应;(2)氢气常用燃着的木条检验,现象是气体燃烧,有淡蓝色的火焰;(3)水分解的实质是:每个水分子分成两个氢原子和一个氧原子,然后每两个氢原子结合成一个氢分子;每两个氧原子结合成一个氧分子。
所以答案是:(1)氢气;5毫升;![]() ;分解反应;(2)燃烧着的木条;体燃烧,有淡蓝色的火焰;(3)氢原子、氧原子;一个氧分子;一个氢分子;原子。
;分解反应;(2)燃烧着的木条;体燃烧,有淡蓝色的火焰;(3)氢原子、氧原子;一个氧分子;一个氢分子;原子。
【考点精析】根据题目的已知条件,利用电解水实验和书写化学方程式、文字表达式、电离方程式的相关知识可以得到问题的答案,需要掌握电解水的实验:A.装置―――水电解器B.电源种类---直流电C.加入硫酸或氢氧化钠的目的----增强水的导电性D.化学反应:2H2O=== 2H2↑+ O2↑;注意:a、配平 b、条件 c、箭号.

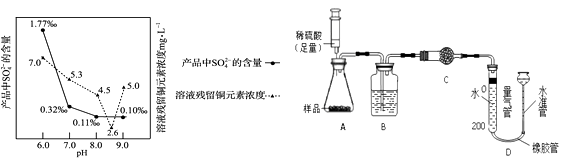
【题目】某化学学习小组借助下列装置(夹持装置已略)及相关试剂粗略测量空气中O2的体积百分数。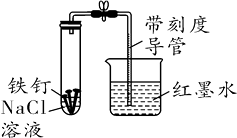
(1)实验前用10%的H2SO4溶液清洗铁钉至有气泡产生。用H2SO4溶液清洗的目的是。写出有关化学方程式。
(2)已知试管剩余空间和导管的体积为40 mL,导管截面积约为1 cm2 , 形成稳定液柱时,读取读数为8.2 cm。则空气中氧气的体积分数为%。
(3)实验时发现上述测量过程因反应较慢耗时较长,对其影响因素作如下分析:
【提出假设】假设一:溶液的pH不同;
假设二:NaCl溶液的浓度不同;
请你再提出一种假设,假设三:不同。
(4)【进行实验】借助上述实验装置,通过取体积、浓度相同NaCl溶液调节溶液的pH获得了如下实验数据:
pH | 2.0 | 5.5 | 6.0 | 6.5 | 7.0 | 8.0 |
液柱高度(cm) | 0 | 1.3 | 8.2 | 8.2 | 8.2 | 8.2 |
形成稳定液柱时间(min) | 3.0 | 3.0 | 5.1 | 5.3 | 15.6 | 17.5 |
【实验结论】根据实验数据分析,为缩短实验测定时间,pH的最佳范围是。
(5)【实验反思】当pH=2时,没有观察到稳定液柱形成的原因是。
(6)请你设计实验,探究NaCl溶液的浓度对铁生锈速率的影响。
实验步骤: 。
实验现象:。