题目内容
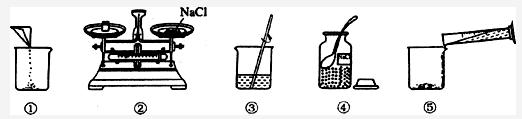
如图是小梅配制100g溶质质量分数为12%的NaCl溶液的实验操作示意图: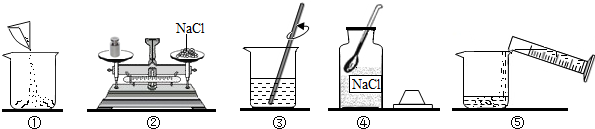
(1)图中的玻璃仪器分别是广口瓶、量筒、烧杯和
(2)指出图中的一处错误操作:
(3)配制时应选择
(4)用上述图示的序号表示配制溶液的操作顺序
(5)将100g溶质质量分数为12%的NaCl溶液变为溶质质量分数为24%的NaCl溶液,应加入

(1)图中的玻璃仪器分别是广口瓶、量筒、烧杯和
玻璃棒
玻璃棒
.(2)指出图中的一处错误操作:
药品与砝码放置错误
药品与砝码放置错误
. (3)配制时应选择
100
100
mL(10mL或50mL或100mL)的量筒量取所需要的水.(4)用上述图示的序号表示配制溶液的操作顺序
④②①⑤③
④②①⑤③
.(5)将100g溶质质量分数为12%的NaCl溶液变为溶质质量分数为24%的NaCl溶液,应加入
15.8
15.8
克溶质或蒸发掉50
50
克水.分析:本题考察的是配制一定溶质质量分数的溶液的实验,在操作时对于天平的使用及实验步骤要求熟记.根据溶质质量分数的计算分式解答.
解答:解:(1)仪器名称为:玻璃棒
(2)托盘天平称量药品时,药品放在左盘,砝码放在右盘,药品与砝码放置错误
(3)配制溶液时所需水的质量为:100g-100g×12%=88g由密度公式可得水的体积为100mL,因此需选择100ml的量筒;
(4)配制溶液的步骤为计算、称量、溶解、装瓶保存.因此顺序为:④②①⑤③
(5)根据溶质质量分数的计算公式可求出加入溶质的质量或蒸发掉水的质量;
故答案为(1)玻璃棒;(2)药品与砝码放置错误(3)100
(4)④②①⑤③
(5)设加入溶质质量为x;24%=
×100% x=15.8g
设蒸发掉水的质量为y,24%=
×100% y=50g
(2)托盘天平称量药品时,药品放在左盘,砝码放在右盘,药品与砝码放置错误
(3)配制溶液时所需水的质量为:100g-100g×12%=88g由密度公式可得水的体积为100mL,因此需选择100ml的量筒;
(4)配制溶液的步骤为计算、称量、溶解、装瓶保存.因此顺序为:④②①⑤③
(5)根据溶质质量分数的计算公式可求出加入溶质的质量或蒸发掉水的质量;
故答案为(1)玻璃棒;(2)药品与砝码放置错误(3)100
(4)④②①⑤③
(5)设加入溶质质量为x;24%=
| 100g×12%+x |
| 100g+x |
设蒸发掉水的质量为y,24%=
| 100g×12% |
| 100g-y |
点评:本题虽然简单,但却训练了学生的实验动手能力.会根据溶质质量分数的计算公式进行计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目