题目内容
由Fe和FeO组成的混合物,测得其中含铁元素的质量分数为80%.取该混合物7g,将其投入适量的稀硫酸中恰好完全反应,所得溶液中溶质的质量为
- A.15.2g
- B.7.6g
- C.20g
- D.40g
A
分析:铁和稀硫酸反应生成硫酸亚铁和氢气,氧化亚铁和稀硫酸反应生成硫酸亚铁和水,因此反应后溶液中的溶质就是硫酸亚铁.根据质量守恒定律可知,反应前后铁元素的质量不变,所以先算出铁元素的质量,然后再计算硫酸亚铁的质量.
解答:铁和稀硫酸反应生成硫酸亚铁和氢气,氧化亚铁和稀硫酸反应生成硫酸亚铁和水,因此反应后溶液中的溶质就是硫酸亚铁.根据质量守恒定律可知,反应前后铁元素的质量不变.混合物中铁元素的质量=7克×80%═5.6克,所以硫酸亚铁中铁元素的质量就是5.6克.硫酸亚铁中铁元素的质量分数=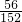 ×100%,所以硫酸亚铁的质量=5.6÷
×100%,所以硫酸亚铁的质量=5.6÷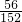 ═15.2克,故选A.
═15.2克,故选A.
点评:掌握质量守恒定律的内涵(化学反应前后元素的种类、质量均不变),注意:铁和氧化亚铁与稀硫酸都反应生成硫酸亚铁.
分析:铁和稀硫酸反应生成硫酸亚铁和氢气,氧化亚铁和稀硫酸反应生成硫酸亚铁和水,因此反应后溶液中的溶质就是硫酸亚铁.根据质量守恒定律可知,反应前后铁元素的质量不变,所以先算出铁元素的质量,然后再计算硫酸亚铁的质量.
解答:铁和稀硫酸反应生成硫酸亚铁和氢气,氧化亚铁和稀硫酸反应生成硫酸亚铁和水,因此反应后溶液中的溶质就是硫酸亚铁.根据质量守恒定律可知,反应前后铁元素的质量不变.混合物中铁元素的质量=7克×80%═5.6克,所以硫酸亚铁中铁元素的质量就是5.6克.硫酸亚铁中铁元素的质量分数=
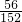 ×100%,所以硫酸亚铁的质量=5.6÷
×100%,所以硫酸亚铁的质量=5.6÷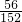 ═15.2克,故选A.
═15.2克,故选A.点评:掌握质量守恒定律的内涵(化学反应前后元素的种类、质量均不变),注意:铁和氧化亚铁与稀硫酸都反应生成硫酸亚铁.

练习册系列答案
相关题目
由Fe和FeO组成的混合物,测得其中含铁元素的质量分数为80%.取该混合物7g,将其投入适量的稀硫酸中恰好完全反应,所得溶液中溶质的质量为( )
| A、15.2g | B、7.6g | C、20g | D、40g |
由Fe和FeO组成的混合物中,测得其中铁元素的质量分数为80%,取该混合物14g,加入足量稀硫酸完全溶解,则反应后溶液中溶质的质量为( )
| A、40g | B、80g | C、15.2g | D、30.4g |