题目内容
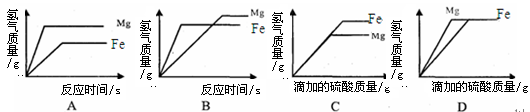
等质量、等质量分数的两份稀硫酸分别于足量的镁和锌反应,则产生的氢气质量( )
| A.镁反应得到多 | B.锌反应得到多 |
| C.一样多 | D.无法确定 |
A
试题分析:足量硫酸,说明金属完全反应.由于都是二价金属,则设金属为M,相对原子质量为x,生成的氢气的质量为y,金属的质量为m.
M+H2SO4=MSO4+H2↑
x 2
m y
y=
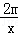
即反应得到的氢气的质量与金属的相对原子质量成反比,由于镁的相对原子质量小,所以对应生成的氢气就多;

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目