题目内容
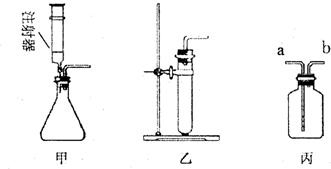
“用双氧水和二氧化锰制氧气”的实验,某同学做了该实验后,展开了下列思考与探究:
(1)催化剂MnO2的用量对反应速率有没有影响呢?他做了这样一组实验:每次均用30 mL 10%的H202溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500 mL氧气时所用的时间,结果如下:(其他实验条件均相同)

请分析表中数据回答:MnO2的用量对反应速率有没有影响呢?如果有,是怎样影响的呢?
答:___________________.
(2)H2O2溶液的溶质质量分数对反应速率有没有影响呢?他又做了一组实验:每次均取5 mL 30%的H2O2溶液,然后稀释成不同溶质质量分数的溶液进行实验,每次所用二氧化锰的质量均为0.2克.记录数据如下:(实验均在20℃室温下进行,其他实验条件也均相同)
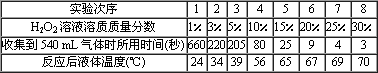
请分析表中数据回答:H2O2溶液的溶质质量分数对反应速率有没有影响呢?如果有,是怎样影响的呢?
答:__________________.
由表中数据还可看出,该反应是个________(填“放热”或“吸热”)反应.
(3)还有哪些因素可能影响该反应的速率呢?
请说出你的一个猜想:________.
答案:
解析:
解析:
|
(1)答:小于0.7 g时,MnO2的用量越大,反应速率越快.当大于0.7 g时,无影响. (2)有,质量分数越大,反应速率越大,放热 (3)环境温度对反应速率有没有影响呢? |

练习册系列答案
相关题目