题目内容
 如图含有少量硫酸钡的氢氧化镁粉末(均匀混合),其中镁元素的质量分数为40%.取该混合物粉末60g与一定量的10%的硫酸恰好完全反应.求:
如图含有少量硫酸钡的氢氧化镁粉末(均匀混合),其中镁元素的质量分数为40%.取该混合物粉末60g与一定量的10%的硫酸恰好完全反应.求:(1)60g混合粉末中硫酸钡的质量为
(2)反应后所得溶液的溶质质量分数?(计算结果保留一位小数)
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:根据镁元素的质量分数可以计算混合物中氢氧化镁的质量,根据氢氧化镁的质量可以计算硫酸钡的质量和反应生成硫酸镁的质量,进一步可以计算反应后所得溶液的溶质质量分数.
解答:解:(1)设氢氧化镁的质量为x,
x×
×100%=60g×40%,
x=58g,
60g混合粉末中硫酸钡的质量为:60g-58g=2g,
故填:2;
(2)设反应的硫酸质量为z,生成硫酸镁的质量为y,
Mg(OH)2+H2SO4=MgSO4+2H2O,
58 98 120
58g z y
=
=
,
y=120g,z=98g,
稀硫酸的质量为:98g÷10%=980g,
反应后所得溶液的溶质质量分数为:
×100%=11.6%,
答:反应后所得溶液的溶质质量分数为11.6%.
x×
| 24 |
| 58 |
x=58g,
60g混合粉末中硫酸钡的质量为:60g-58g=2g,
故填:2;
(2)设反应的硫酸质量为z,生成硫酸镁的质量为y,
Mg(OH)2+H2SO4=MgSO4+2H2O,
58 98 120
58g z y
| 58 |
| 58g |
| 98 |
| z |
| 120 |
| y |
y=120g,z=98g,
稀硫酸的质量为:98g÷10%=980g,
反应后所得溶液的溶质质量分数为:
| 120g |
| 58g+980g |
答:反应后所得溶液的溶质质量分数为11.6%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
图中盛装块状烧碱的集气瓶还可以盛装下列哪些物质得到的结果一样( )
| A、石灰石 | B、生石灰 |
| C、孰石灰 | D、石灰水 |
 随着人们生活水平的提高,哈尔滨市私家车数量不断增加,提高了人们的生活质量,给大家出行带来了很多方便.请回答下列问题:
随着人们生活水平的提高,哈尔滨市私家车数量不断增加,提高了人们的生活质量,给大家出行带来了很多方便.请回答下列问题: 黑龙江省是我国生产粮食的大省,每年为国家提供了大量的粮食,被称为东北大粮仓.请回答下列问题:
黑龙江省是我国生产粮食的大省,每年为国家提供了大量的粮食,被称为东北大粮仓.请回答下列问题:
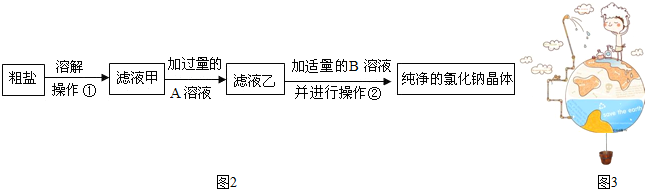
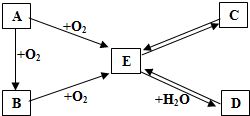 A、B、C、D、E是初中化学中常见的不同物质,其中A为黑色固体单质,C为难溶性钙盐.其转化关系如图所示:
A、B、C、D、E是初中化学中常见的不同物质,其中A为黑色固体单质,C为难溶性钙盐.其转化关系如图所示: