题目内容
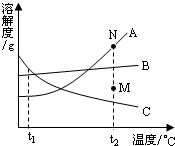
 右图是物质A、B、C的溶解度曲线.下列相关说法正确的是
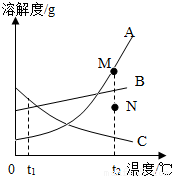
右图是物质A、B、C的溶解度曲线.下列相关说法正确的是
- A.t2℃时,A、B、C三种物质的溶解度大小关系是C>B>A
- B.将t2℃时A、B、C的饱和溶液冷却到t1℃,所得的三种溶液中A溶液的溶质质量分数最小
- C.若要将M点的A溶液转变为N点的A溶液,只能采取恒温蒸发溶剂的方法
- D.将t2℃时M点的C固体与水的混合物降温到t1℃,可得到C的不饱和溶液
D
分析:A、根据溶解度曲线判断同一温度时不同物质的溶解度大小;
B、将t2℃时A,B,C的饱和溶液冷却到t1℃,A和B都会析出晶体,使溶液中溶质质量分数变小,但C物质不会析出晶体,溶质的质量分数不变,而t1℃时B的溶解度>t1℃时A的溶解度>t2℃时C的溶解度,所以所得的三种溶液中溶质的质量分数B>A>C;
C、溶解度曲线上的点表示该温度下此物质的溶液处于饱和状态,下部的点表示该温度下此物质的溶液处于不饱和状态;
D、根据溶解度曲线以上面积的点,表示该温度下此物质的溶液处于饱和状态,且溶质有剩余,以及C点的溶解度曲线变化分析解答.
解答:A、观察图示可知:t2℃时A、B、C三种物质的溶解度大小关系是A>B>C,故错误;
B、将t2℃时A,B,C的饱和溶液冷却到t1℃,所得的三种溶液中溶质的质量分数B>A>C,故错误;
C、若要将组成在M点的A溶液转变为N点的溶液,即将A由不饱和溶液变为饱和溶液,除了采取恒温蒸发溶剂的方法,还可以采取增加溶质的方法;故题目说法错误;
D、因为t1℃时C物质的溶解度比M点溶质质量大,所以t2℃时M点的C与水的混合物降温到t1℃,C由饱和溶液变为不饱和溶液,故正确;
故选D.
点评:本题主要考查了固体溶解度曲线的点、溶解度变化趋势所表示的意义,及对固体溶解度概念的理解,饱和溶液和不饱和溶液的相互转化,培养了学生的理解能力和应用能力.
分析:A、根据溶解度曲线判断同一温度时不同物质的溶解度大小;
B、将t2℃时A,B,C的饱和溶液冷却到t1℃,A和B都会析出晶体,使溶液中溶质质量分数变小,但C物质不会析出晶体,溶质的质量分数不变,而t1℃时B的溶解度>t1℃时A的溶解度>t2℃时C的溶解度,所以所得的三种溶液中溶质的质量分数B>A>C;
C、溶解度曲线上的点表示该温度下此物质的溶液处于饱和状态,下部的点表示该温度下此物质的溶液处于不饱和状态;
D、根据溶解度曲线以上面积的点,表示该温度下此物质的溶液处于饱和状态,且溶质有剩余,以及C点的溶解度曲线变化分析解答.
解答:A、观察图示可知:t2℃时A、B、C三种物质的溶解度大小关系是A>B>C,故错误;
B、将t2℃时A,B,C的饱和溶液冷却到t1℃,所得的三种溶液中溶质的质量分数B>A>C,故错误;
C、若要将组成在M点的A溶液转变为N点的溶液,即将A由不饱和溶液变为饱和溶液,除了采取恒温蒸发溶剂的方法,还可以采取增加溶质的方法;故题目说法错误;
D、因为t1℃时C物质的溶解度比M点溶质质量大,所以t2℃时M点的C与水的混合物降温到t1℃,C由饱和溶液变为不饱和溶液,故正确;
故选D.
点评:本题主要考查了固体溶解度曲线的点、溶解度变化趋势所表示的意义,及对固体溶解度概念的理解,饱和溶液和不饱和溶液的相互转化,培养了学生的理解能力和应用能力.

练习册系列答案
相关题目
 19、右图是物质A、B、C的溶解度曲线,下列相关说法正确的是( )
19、右图是物质A、B、C的溶解度曲线,下列相关说法正确的是( )