题目内容
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答:
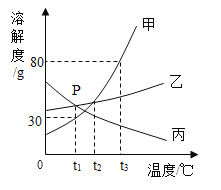
(1)P 点表示的含义是______________。
(2)当甲中含有少量乙时,提纯甲的方法是___________________。
(3)要使接近饱和的丙溶液变为饱和溶液,可采取的措施有(任写一种)_______________。
(4)t1℃时,将 30g 甲物质投入到 50g 水中充分溶解后,所得溶液的质量为_________g;若将温度升至 t3 ℃,使所得溶液的溶质质量分数变为 20%,应该再加水___________g。
(5)t3 ℃时,取等质量的甲、乙、丙三种物质分别配制成饱和溶液,需要水的质量最小的是_________。
(6)t3 ℃时,将等质量的三种物质的饱和溶液降温到 t2℃,对所得溶液的叙述正确的是_______________(填字母)。
A 溶液的质量关系是丙>乙>甲
B 丙溶液的溶质质量分数不变
C 溶剂的质量关系是甲=乙>丙
【答案】t1℃时,乙、丙的溶解度相等 降温结晶或冷却热饱和溶液 升温(或增加溶质) 65 70 甲 AB
【解析】
(1)通过分析溶解度曲线可知,曲线中P点含义是:t1℃时,乙、丙的溶解度相等;
(2)甲的溶解度随温度的升高变化明显,且随温度升高而迅速增大,而乙的溶解度受温度影响很小,故当甲中含有少量乙时,提纯甲的方法是降温结晶(或冷却热饱和溶液);
(3)丙的溶解度随温度的升高而减小,要使接近饱和的丙溶液变为饱和溶液,可采取的措施有升高温度或增加溶质;
(4)t1℃时甲的溶解度是30g,50g水中最多溶解15g甲物质,所以将30g加入到50g水中,所得溶液的质量是65g;t3℃时甲的溶解度是80g,将30g加入到50g水中可完全溶解,所得溶液的质量为80g,使所得溶液的溶质质量分数变为 20%,设应再加水的质量为x,
(80g+x)×20%=30g,x=70g;
(5)t3℃时,甲物质的溶解度最大,所以取等质量的甲、乙、丙三种物质分别配制成饱和溶液,需要水的质量最小的是甲;
(6)t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至t1℃。
A.由溶解度曲线可知,降温到t2℃,析出晶体最多的是甲,然后是乙,而丙没有晶体析出,故溶液的质量关系是丙>乙>甲,故正确;
B.丙物质的溶解度随温度的升高而减小,故降低温度没有晶体析出,溶质质量分数不变,故正确;
C.降温过程中溶剂的质量不变,t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液,溶解度大的需要水少,故溶剂质量关系甲<乙<丙,故错误;
故选AB。

【题目】下列物质鉴别方案正确的是( )
选项 | 鉴别物质 | 实验方案 |
A | 氯化钠溶液、碳酸钠溶液、氢氧化钠溶液 | 用酚酞溶液 |
B | Fe2(SO4)3、NaOH、NaNO3、HCl 四种溶液 | 仅用组内物质鉴别 |
C | 尿素、氯化铵、硝酸铵 | 加熟石灰研磨闻气味 |
D |
| 用燃着的木条 |
A.AB.BC.CD.D
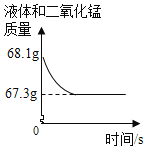
【题目】利用沉淀法可测定某粗盐样品的纯度(假定粗盐中的杂质全部是MgCl2)。每次取100 g样品配制成溶液,向其中加入质量分数为10%的氢氧化钠溶液,测得生成沉淀的质量与所加氢氧化钠溶液的质量关系如下表所示:
测定次数 | 第一次 | 第二次 | 第三次 | 第四次 |
样品质量/g | 100 | 100 | 100 | 100 |
氢氧化钠溶液质量/g | 32 | 64 | 82 | 90 |
沉淀质量/g | 2.32 | 4.64 | 5.8 | 5.8 |
(1)求粗盐的纯度________。
(2)当样品与所加氢氧化钠溶液恰好完全反应时,求溶液中氯化钠的质量________。(写出解题过程)
【题目】某校同学开展了如图所示的“溶液酸碱性的检验”的实验活动.
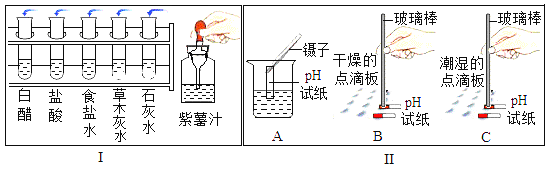
(1)把自制的紫色紫薯汁按图![]() 所示分别滴加到试管中,观察到的现象如下表所示:
所示分别滴加到试管中,观察到的现象如下表所示:
溶液 | 白醋 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
加入紫薯汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
①图![]() 中存放紫薯汁的仪器名称为________.
中存放紫薯汁的仪器名称为________.
②根据上表推测,紫薯汁能作酸碱指示剂,遇到稀硫酸可能显示的颜色是________.
(2)用pH试纸测定图![]() 中部分溶液的酸碱度:草木灰水
中部分溶液的酸碱度:草木灰水![]() ,属于________
,属于________![]() 填“酸性”“中性”或“碱性”
填“酸性”“中性”或“碱性”![]() 溶液;白醋pH________
溶液;白醋pH________![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() .
.
(3)图![]() 是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是________
是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是________![]() 填“A”“B”或“C”,下同
填“A”“B”或“C”,下同![]() ,可能导致所测溶液pH发生改变的错误操作是________,如果测定的是石灰水,测得的pH将________
,可能导致所测溶液pH发生改变的错误操作是________,如果测定的是石灰水,测得的pH将________![]() 填“偏大”“不变”或“偏小”
填“偏大”“不变”或“偏小”![]() 简述正确测定溶液PH的操作步骤:________.
简述正确测定溶液PH的操作步骤:________.