题目内容
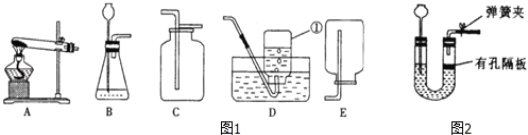
【题目】如图是某研究性学习小组进行CO2与NaOH溶液反应的探究实验装置.
【查阅资料】水的沸点与气体压强有关,气体压强小,沸点低;气体压强大,沸点高.
【实验探究】实验步骤如下:
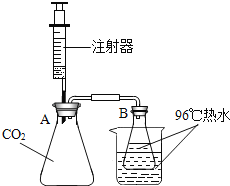
步骤①:如图所示,锥形瓶A盛满CO2气体,锥形瓶B盛有96%以上但未沸腾的热水,烧杯中加入同样温度的热水(起保持锥形瓶B中水温恒定的作用).
步骤②:取2支注射器,一支抽取20mL水,另一支抽取20mL浓NaOH溶液.
步骤③:将注射器中20mL水注入锥形瓶A中,振荡后观察,锥形瓶B中的热水没有沸腾.
步骤④:取下盛水的注射器,再将盛20mL浓NaOH溶液的注射器迅速连接到锥形瓶A上,注入该溶液并振荡,观察到明显的现象.
请回答下列问题:
(1)实验开始前,依上图连接好装置(锥形瓶A、B和烧杯均未盛装物质),将一支空注射器连接到锥形瓶A上,并将其活塞缓慢向上拉,几秒钟后松手,观察活塞是否复位,这个操作的目的是 .
(2)锥形瓶A中CO2与NaOH溶液反应的化学方程式是 .
(3)步骤④锥形瓶B中产生的明显现象是 ;产生明显现象的原因是 .
【答案】(1)检查装置气密性;(2)2NaOH+CO2═Na2CO3+H2O;(3)水沸腾;B中气压减小,水的沸点降低;
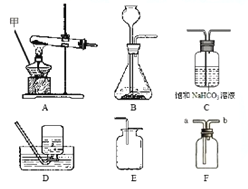
【解析】(1)用注射器检查装置的气密性,首先向锥形瓶中加入少量水,浸没长颈漏斗下端,然后将注射器C连接到装置E的导管口处,缓慢拉动注射器C的活塞,观察到长颈漏斗下端有气泡冒出,说明装置的气密性良好;
(2)由于二氧化碳可以和氢氧化钠溶液发生反应,生成碳酸钠的水,其化学方程式为:2NaOH+CO2═Na2CO3+H2O;
(3)氢氧化钠与锥形瓶A中的CO2气体反应,生成碳酸钠和水,使瓶中气压减小,水的沸点降低,故接近沸腾的水会开始沸腾;

【题目】为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小鸣和同学们通过测定了反应后溶液的pH,得到了如右图所示的pH曲线,请回答:

(1)由图可知该实验操作是将 滴加到另一种溶液中;
(2)该反应的化学方程式为 ;
(3)实验过程中,小鸣取了a、b、c三处反应后的溶液于三个烧杯中,却忘了作标记,请你设计不同的方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液。
![]() 【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3=CaCO3↓+2NaCl。
【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3=CaCO3↓+2NaCl。
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现 的现象。结论:该样品是a处溶液。
②为进一步确定b或c处溶液,又设计了以下方案:
实验步骤 | 实验现象 | 实验结论 |
另取余下样品少量于两支试管中,分别滴加足量的Na2CO3溶液。 | 该样品为b处溶液。 | |
该样品为c处溶液,并推知溶液中的阳离子有 。 |
【反思评价】探究反应后溶液中溶质的成分,除了要考虑生成物之外,还要考虑 。