题目内容
实验室用溶质质量分数为5%的过氧化氢溶液与二氧化锰混合制取氧气.若要制取1.6g氧气,理论上需要该过氧化氢溶液的质量是多少?(请写出计算过程)
【答案】
68g
【解析】
试题分析:设需要过氧化氢的质量x.
2H2O2 2H2O+O2↑
2H2O+O2↑
68 32
x 1.6g
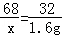
解得:x=3.4g
所以理论上需要该过氧化氢溶液的质量是:3.4g÷5%=68g
答:理论上需要该过氧化氢溶液的质量是68g.
考点:根据化学反应方程式的计算.
点评:利用溶液中溶质质量分数= ×100%,由溶质的质量及溶液的质量分数可计算溶液的质量.
×100%,由溶质的质量及溶液的质量分数可计算溶液的质量.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目