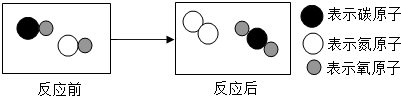
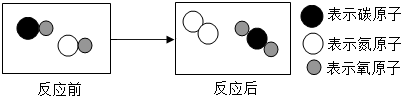
题目内容
两种氧化物的固体混合物共5.6g,跟7.3%的盐酸100g恰好完全反应,则该混合物可能是
- A.MgO和ZnO
- B.CaO和CuO
- C.MgO和CuO
- D.CaO和MgO
AC
分析:根据化学方程式,列出比例式,计算出跟7.3%的盐酸100g恰好完全反应的氧化物中金属的相对原子质量的取值范围;然后结合选项逐一分析,即可正确选择.
解答:设跟7.3%的盐酸100g恰好完全反应的氧化物的化学式为RO,R的相对原子质量为x,则化学方程式为:
RO+2HCl=RCl2+H20
x+16,73
5.6g,7.3%×100g
∴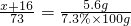
解之得:x=40,
故两种氧化物中,金属的相对原子质量应该一个大于40,一个小于40,
A、Mg的相对原子质量为24<40,Zn的相对原子质量为65>40,故A适合;
B、Ca的相对原子质量为40,Cu的相对原子质量为64,不满足一个大于40,一个小于40的要求.故B不适合;
C、Mg的相对原子质量为24<40,Cu的相对原子质量为64>40,故C适合;
D、Ca的相对原子质量为40,Mg的相对原子质量为24<40,故D不适合.
故选AC.
点评:本题主要考查学生灵活运用化学方程式和元素的相对原子质量综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
分析:根据化学方程式,列出比例式,计算出跟7.3%的盐酸100g恰好完全反应的氧化物中金属的相对原子质量的取值范围;然后结合选项逐一分析,即可正确选择.
解答:设跟7.3%的盐酸100g恰好完全反应的氧化物的化学式为RO,R的相对原子质量为x,则化学方程式为:
RO+2HCl=RCl2+H20
x+16,73
5.6g,7.3%×100g
∴
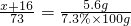
解之得:x=40,
故两种氧化物中,金属的相对原子质量应该一个大于40,一个小于40,
A、Mg的相对原子质量为24<40,Zn的相对原子质量为65>40,故A适合;
B、Ca的相对原子质量为40,Cu的相对原子质量为64,不满足一个大于40,一个小于40的要求.故B不适合;
C、Mg的相对原子质量为24<40,Cu的相对原子质量为64>40,故C适合;
D、Ca的相对原子质量为40,Mg的相对原子质量为24<40,故D不适合.
故选AC.
点评:本题主要考查学生灵活运用化学方程式和元素的相对原子质量综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目