题目内容
我国科学家研制出具有自主知识产权的国产芯片“龙芯”一号和“龙芯”二号,其芯片的核心部件是以高纯硅单质(Si)为原料制成的.用化学方法制备高纯硅的化学反应方程式是X+2H2 Si+4HCl.
Si+4HCl.(1)推断X的化学式为______.
(2)计算要获得56g硅单质(Si),至少需要氢气多少克?
【答案】分析:(1)根据反应前后各原子种类和数目不变求出化学式;(2)通过方程式列比例式由硅质量计算出氢气质量即可.
解答:解:(1)生成物中含有1个硅原子,4个氢原子,4个氯原子,反应物中已经含有4个氢原子,还缺少1个硅原子,4个氯原子,所以X的化学式为:SiCl4;
(2)解:设至少需要氢气的质量为x.
SiCl4+2H2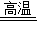 Si+4HCl
Si+4HCl
4 28
x 56 g
根据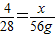 解得x=8 g
解得x=8 g
答:至少需要氢气的质量是8 g.
故答案为:(1)SiCl4;(2)8g.
点评:要熟记质量守恒定律内容并能灵活运用回答相应问题.
解答:解:(1)生成物中含有1个硅原子,4个氢原子,4个氯原子,反应物中已经含有4个氢原子,还缺少1个硅原子,4个氯原子,所以X的化学式为:SiCl4;
(2)解:设至少需要氢气的质量为x.
SiCl4+2H2
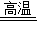 Si+4HCl
Si+4HCl4 28
x 56 g
根据
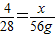 解得x=8 g
解得x=8 g答:至少需要氢气的质量是8 g.
故答案为:(1)SiCl4;(2)8g.
点评:要熟记质量守恒定律内容并能灵活运用回答相应问题.

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
 学科间综合题:目前,化石燃料是人类生产、生活的主要能源.随着全球能量使用的增长,化石燃料等不可再生能源将日趋枯竭.世界各国人民的节能意识也日趋增强(如图)是我国的节能标志,科学家也在开发新能源、研制节能产品、提高化学能的转化效率等方面,做着积极的努力.请你回答:
学科间综合题:目前,化石燃料是人类生产、生活的主要能源.随着全球能量使用的增长,化石燃料等不可再生能源将日趋枯竭.世界各国人民的节能意识也日趋增强(如图)是我国的节能标志,科学家也在开发新能源、研制节能产品、提高化学能的转化效率等方面,做着积极的努力.请你回答: 目前,化石燃料是人类生产、生活的主要能源.随着全球能量使用的增长,化石燃料等不可再生能源将日趋枯竭.世界各国人民的节能意识正在日趋增强(如图是我国的节能标志),科学家也在开发新能源、研制节能产品、提高化学能的转化效率等方面,做着积极的努力.请你回答:
目前,化石燃料是人类生产、生活的主要能源.随着全球能量使用的增长,化石燃料等不可再生能源将日趋枯竭.世界各国人民的节能意识正在日趋增强(如图是我国的节能标志),科学家也在开发新能源、研制节能产品、提高化学能的转化效率等方面,做着积极的努力.请你回答: 目前化石燃料是人类生产、生活的主要能源.随着全球能量使用的增长,化石燃料等不可再生能源将日趋枯竭,世界各国人民的节能意识正在日趋增强(右图是我国的节能标志),科学家也在开发新能源、研制节能产品,提高化学能的转化效率等方面做着积极的努力.
目前化石燃料是人类生产、生活的主要能源.随着全球能量使用的增长,化石燃料等不可再生能源将日趋枯竭,世界各国人民的节能意识正在日趋增强(右图是我国的节能标志),科学家也在开发新能源、研制节能产品,提高化学能的转化效率等方面做着积极的努力. 目前,化石燃料是人类生产、生活的主要能源.随着全球能量使用的增长,化石燃料等不可再生能源将日趋枯竭.世界各国人民的节能意识正在日趋增强(如图是我国的节能标志),科学家也在开发新能源、研制节能产品、提高化学能的转化效率等方面做着积极的努力.请回答:
目前,化石燃料是人类生产、生活的主要能源.随着全球能量使用的增长,化石燃料等不可再生能源将日趋枯竭.世界各国人民的节能意识正在日趋增强(如图是我国的节能标志),科学家也在开发新能源、研制节能产品、提高化学能的转化效率等方面做着积极的努力.请回答: