题目内容
【题目】实验室用溶质质量分数为10%氢氧化钠溶液进行水的电解实验。
【实验一】配制溶质质量分数为10%氢氧化钠溶液100g。
(1)所需的氢氧化钠质量______g;需要水的质量______,体积为______ ml(水的密度为1g/cm3)。量水时若仰视读数,则配得溶液的溶质质量分数将______ (“偏大”或“偏小”)。
(2)称量时,氢氧化钠固体应放于天平______(填“左”或“右”)盘的烧杯内;量取所需要的水(水的密度为1g/cm3),应选择的量筒的规格是______ml(选填“10”、“100”或“250”)。
【实验二】水的电解实验
用如图装置进行水的电解实验。已知氢氧化钠在水的电解实验中,只起到增强水的导电性作用。
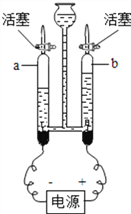
(3)开始反应前a,b两管内都充满溶液。关闭活塞,接通电源,一段时间后,两管产生的气体如图所示,则a管中的气体是______,可以用____________来检验。b管中的气体用______验证,现象为 __________________。写出电解水的化学方程式________________。
(4)电解后溶液的溶质质量分数______10%(填“<”、“=”或“>”)。
【答案】 10 90g 90 偏小 左 100 氢气(或H2) 燃着的木条 带火星的木条 【答题空10】带火星的木条复燃 2H2O![]() 2H2 ↑ +O2↑ >
2H2 ↑ +O2↑ >
【解析】【实验一】配制溶质质量分数为10%氢氧化钠溶液100g。(1)所需的氢氧化钠质量![]() ;需要水的质量为100g-10g=90g,水的密度为1g/cm3,体积为90ml,量水时若仰视读数,读数偏小,实际体积偏大,则配得溶液的溶质质量分数将偏小;(2)称量时,氢氧化钠固体应放于天平左盘的烧杯内;量取所需要的水(水的密度为1g/cm3),应选择的量筒的规格是100ml;(3)电解水时,负极产生的较多气体是氢气,可以用燃着的木条来检验,氢气燃烧,产生淡蓝色火焰,有水珠生成,正极产生的是氧气,可以用带火星的木条验证,现象为:带火星的木条复燃;电解水生成氢气和氧气,化学方程式为:2H2O
;需要水的质量为100g-10g=90g,水的密度为1g/cm3,体积为90ml,量水时若仰视读数,读数偏小,实际体积偏大,则配得溶液的溶质质量分数将偏小;(2)称量时,氢氧化钠固体应放于天平左盘的烧杯内;量取所需要的水(水的密度为1g/cm3),应选择的量筒的规格是100ml;(3)电解水时,负极产生的较多气体是氢气,可以用燃着的木条来检验,氢气燃烧,产生淡蓝色火焰,有水珠生成,正极产生的是氧气,可以用带火星的木条验证,现象为:带火星的木条复燃;电解水生成氢气和氧气,化学方程式为:2H2O![]() 2H2
2H2![]() +O2
+O2![]() ;(4)电解后氢氧化钠质量不变,溶液质量减小,因此溶液的溶质质量分数变大。
;(4)电解后氢氧化钠质量不变,溶液质量减小,因此溶液的溶质质量分数变大。

