题目内容
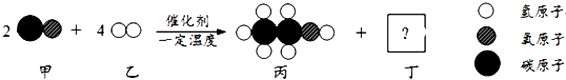
【题目】一个密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得数据见下表。下列说法中正确的是

A. X=7 g B. 该反应是分解反应
C. 在该反应中,丙物质一定做催化剂 D. 在该反应的化学方程式中,丙、丁的化学计量数之比为l:l
【答案】A
【解析】A、根据质量守恒定律,8+35+5+8=2+x+5+42得x=7,正确;
B、由表可知,甲物质质量减少,是反应物,乙物质质量减少,也是反应物,丁物质质量增加是生成物,故该反应为化合反应,错误;
C、在反应中丙物质的质量没有发生变化,丙物质可能是催化剂,也可能是不参加反应的杂质,错误;
D、该反应中不知道各物质的相对分子质量,故没办法知道计量数比,错误。故选A。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】我国劳动人民早在五千年前就会使用木炭炼铜.在化学实验室里模拟炼铜,既可用传统的实验装置(见图甲),又能用改进的微型实验装置(见图乙).化学兴趣小组采用图乙装置,开展以下探究活动
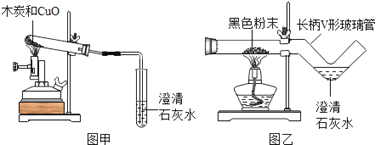
【提出问题】木炭与CuO反应所得红色固体中含有什么物质?
【查阅资料】
(1)木炭与CuO的反应是:C+2CuO![]() 2Cu+CO2↑,若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O).
2Cu+CO2↑,若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O).
(2)Cu2O是红色固体,能与稀硫酸反应:Cu2O+H2SO4═Cu+CuSO4+H2O
【作出猜想】红色固体的成分:①全部是Cu;②全部是Cu2O;③ .
【实验探究】
(1)取木炭、CuO两种黑色粉末适量,再也少许CaC12(能降低反应温度,加快反应速率)均匀混合,然后将黑色粉末装入长柄V形玻璃管的直管内.
(2)按图乙连好实验装置,然后加热反应物;2分钟后,黑色粉末出现红热现象,同时澄清的石灰水 ,此时停止加热.
(3)待玻璃管冷却后,提取里面的红色固体,进行如下的验证:
步骤 | 现象 | 结论 |
①取1.44g红色固体装入试管,滴入足量的 ,充分反应 | 红色固体部分减少,溶为变 | 猜想 错误 |
②滤了试管中残留的红色固体,洗涤干燥,称其质量为1.04g | / | 猜想 正确 |
【评价反思】
(1)使用图乙装置与使用图甲装置相比,其优点是 (写出1条即可).
(2)若要证明CaC12是该反应的催化剂,还需要验证CaCl2的 .
(3)在铜的冶炼史中,我国劳动人民还有一项重大发明就是“湿法炼铜”,该方法可用化学方程式表示为 .