题目内容
【题目】水和溶液在生产生活中重要的作用.
(1)自来水厂常用的净水方法有沉淀、_____、吸附、消毒等,吸附过程中需要用到的物质是_____;在日常生活中鉴别硬水和软水常用_____,常用来降低水的硬度的方法是_____,水是一种宝贵的自然资源,我们必须爱护水资源.预防水污染的措施有_____(写一条即可).
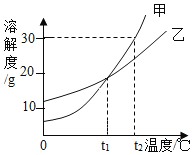
(2)如图是甲、乙两种物质的溶解度曲线,回答下列问题:
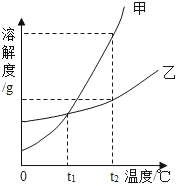
①t1℃时,甲、乙两种溶液中溶质的质量分数一定相等_____(填“对”或“错”);
②若固体甲中含有少量乙时可用_____方法提纯甲(填“蒸发结晶”或“冷却结晶”);
③t2℃用等质量的甲、乙两种物质配制甲、乙的饱和溶液需要水的质量甲_____乙(填“>”“<”或“=”);
④配制一定溶质质量分数的甲物质溶液,以下操作中会导致所配制溶液溶质质量分数偏低的是_____.
A 量筒量取水时仰视读数 B 配制好的溶液向细口瓶转移时溅出 C 固体甲中含有杂质.
【答案】过滤 活性炭 肥皂水 煮沸 污水处理后排放 错 冷却结晶 < AC
【解析】
(1)自来水厂常用的净水方法有沉淀、过滤、吸附、消毒等,吸附过程中需要用到的物质是活性炭;在日常生活中鉴别硬水和软水常用肥皂水,常用来降低水的硬度的方法是煮沸,水是一种宝贵的自然资源,我们必须爱护水资源,预防水污染的措施有:污水处理后排放;
(2)①t1℃时,甲、乙两种饱和溶液中溶质的质量分数一定相等,故错;②甲物质的溶解度受温度变化影响较大,所以固体甲中含有少量乙时可用冷却结晶方法提纯甲;
③t2℃,甲物质的溶解度大于乙物质的溶解度,所以用等质量的甲、乙两种物质配制甲、乙的饱和溶液需要水的质量甲<乙;
④A、量筒量取水时仰视读数,水的体积偏大,所以溶液溶质质量分数偏低,故A正确;B、溶液具有均一性,配制好的溶液向细口瓶转移时溅出,不会影响溶质的质量分数,故B错误;C、固体甲中含有杂质,氯化钠的实际质量偏小,所以溶液溶质质量分数偏低,故C正确。
故选:AC.

【题目】火锅是我国独创的美食,历史悠久。火锅常用的一种燃料是固体酒精。某化学兴趣小组的同学对“固体酒精”产生了好奇,对其成分进行探究。请你回答下列问题。
(查阅资料)
a.固体酒精也被称为"酒精块"或固体燃料块。固体酒精并不是固体状态的酒精而是将酒精、硬脂酸和氢氧化钠按一定的质量比混合制成。
b.酒精的化学式为C2H5OH;
c.氯化钡、氯化钠溶液均呈中性。
d. BaCl2+Na2CO3=BaCO3↓+2NaCl 生成的BaCO3为白色固体
(提出问题)
(1)酒精的化学式与NaOH相比,都有“OH”,那么酒精的水溶液是不是显碱性?
(2)固体酒精中的氢氧化钠是否变质及变质的程度如何?
(实验探究1)酒精的水溶液是不是显碱性
同学们取少量酒精溶液于试管中,滴加紫色石蕊溶液,未观察到紫色石蕊变为蓝色,说明酒精溶液_______(填“显”或“不显”)碱性。
(实验探究2)固体酒精中的氢氧化钠是否变质及变质的程度如何
①固体酒精中的氢氧化钠是否变质,同学们先取少量固体酒精于烧杯中,加入足量水溶解后滴加足量的稀盐酸,观察到__________现象,说明氢氧化钠已变质.请写出氢氧化钠在空气中变质的化学方程式______________。
②为进一步确定氢氧化钠的变质程度,分组进行探究。
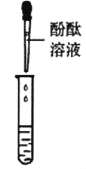
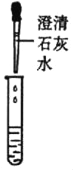
甲组同学取烧杯上层清液于两支试管中,按如图所示进行实验。
实验方案 |
|
|
实验现象 | 溶液变红 | 产生__ |
实验结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
乙组同学认为甲组实验不能证明清液中一定有氢氧化钠,理由是__。他们另取烧杯中上层清液,加足量氯化钡溶液,充分反应后,静置,取上层清液,滴加酚酞溶液,酚酞溶液变红。
(反思交流)乙组实验中加足量氯化钡溶液的目的是________。
(实验结论]小组同学经过讨论,一致认为该固体酒精中的氢氧化钠部分变质。