��Ŀ����
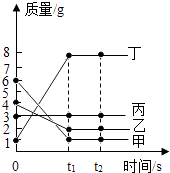
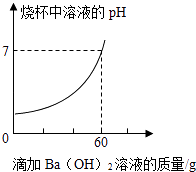
����Ŀ��ijƷ�ƽ����ijɷ�������������Ļ����Һ��ij����С����ⶨ��Ʒ�ƽ������Һ��HCl��������ȡ20g��Ʒ�ƵĽ������Һ���ձ��У����ϵμ�������������Ϊ17.1%������������Һ����Ӧ�������ձ��в��������������ձ�����ҺpHֵ�仯�IJ������������ʾ������֪BaCl2��Һ��pH=7��
�μ�����������Һ������/g | 5 | 10 | 25 | 30 |
�ձ��в�������������/g | 1.165 | 2.33 | 4.66 | 4.66 |
��
��1����ȫ��Ӧ�����ɳ���������Ϊ��
��2������ý������Һ��HCl����������Ϊ���٣���������������0.1%��
���𰸡�
��1��4.66
��2���⣺����H2SO4��Ӧ��Ba��OH��2����Ϊx��
Ba��OH��2+H2SO4= | BaSO4��+2H2O |
171 | 233 |
x | 4.66g |
![]() ��ã�x=3.42g
��ã�x=3.42g
����H2SO4��Ӧ��Ba��OH��2��Һ����Ϊ�� ![]() =20g��
=20g��
����HCl��ȫ��Ӧ��Ba��OH��2��Һ������Ϊ��60g��20g=40g��
��20g��Ʒ�ƽ������Һ��HCl������Ϊy��
Ba��OH��2+ | 2HCl=BaCl2+2H2O |
171 | 73 |
40g��17.1% | y |
![]() ��ã�y=2.92g
��ã�y=2.92g
�ý������Һ��HCl����������Ϊ�� ![]() =14.6%
=14.6%
�𣺼���ý������Һ��HCl����������Ϊ14.6%
���������⣺��1���������֪��H2SO4��ȫ��Ӧ�����BaSO4������������4.66g���𣺣�1��4.66�� ����������������Һ��Ӧ�����Ȼ�����ˮ������������������Һ��Ӧ�������ᱵ������ˮ����ͼʾ��֪��ǡ����ȫ��Ӧʱ�����ĵ�����������Һ������Ϊ60g�������ij���������Ϊ4.66g���ݴ˽�Ϸ�Ӧ�Ļ�ѧ����ʽ���з�����ɣ�