题目内容
 根据如图溶解度曲线,得到的结论正确的是
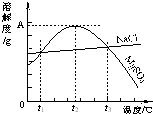
根据如图溶解度曲线,得到的结论正确的是
- A.MgSO4的溶解度随温度升高而增大
- B.只有在t1℃时,NaCl和MgSO4的溶解度才相等
- C.把MgSO4饱和溶液的温度从t2℃降至t1℃时,有晶体析出
- D.MgSO4饱和溶液中溶质的质量分数随温度的升高而增大
C
分析:根据固体物质的溶解度曲线可以:①比较不同物质在同一温度下的溶解度大小,②判断通过降温还是升温的方法使溶质从溶液中结晶析出,③判断物质的溶解度随温度变化的变化情况,④判断采用降温结晶还是蒸发溶剂的方法达到提纯物质的目的等.
解答:A、由各物质的溶解度曲线不难看出,硫酸镁的溶解度先随温度的升高而增大,后随温度的升高而降低,故A错误;
B、在t1℃、t3℃时,NaCl和MgSO4的溶解度相等,故B错误;
C、从t2℃降至t1℃时,硫酸镁的溶解度减小,所以把MgSO4饱和溶液的温度从t2℃降至t1℃时,有晶体析出,故C正确;
D、由各物质的溶解度曲线不难看出,硫酸镁的溶解度先随温度的升高而增大,后随温度的升高而降低,MgSO4饱和溶液中溶质的质量分数随温度的升高而增大到达t2℃后溶质的质量分数又减小,故D错误.
故选C.
点评:本题难度不是很大,主要考查了固体溶解度曲线所表示的意义及根据溶解度曲线解决有关的问题,培养学生分析问题、解决问题的能力.
分析:根据固体物质的溶解度曲线可以:①比较不同物质在同一温度下的溶解度大小,②判断通过降温还是升温的方法使溶质从溶液中结晶析出,③判断物质的溶解度随温度变化的变化情况,④判断采用降温结晶还是蒸发溶剂的方法达到提纯物质的目的等.
解答:A、由各物质的溶解度曲线不难看出,硫酸镁的溶解度先随温度的升高而增大,后随温度的升高而降低,故A错误;
B、在t1℃、t3℃时,NaCl和MgSO4的溶解度相等,故B错误;
C、从t2℃降至t1℃时,硫酸镁的溶解度减小,所以把MgSO4饱和溶液的温度从t2℃降至t1℃时,有晶体析出,故C正确;
D、由各物质的溶解度曲线不难看出,硫酸镁的溶解度先随温度的升高而增大,后随温度的升高而降低,MgSO4饱和溶液中溶质的质量分数随温度的升高而增大到达t2℃后溶质的质量分数又减小,故D错误.
故选C.
点评:本题难度不是很大,主要考查了固体溶解度曲线所表示的意义及根据溶解度曲线解决有关的问题,培养学生分析问题、解决问题的能力.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目

 (2013?通州区二模)根据如图溶解度曲线,判断下列说法正确的是( )
(2013?通州区二模)根据如图溶解度曲线,判断下列说法正确的是( )

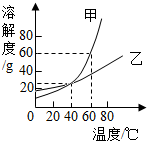 溶解度曲线为我们定量描述物质的溶解性供了便利.请你根据如图溶解度曲线判断下列说法,其中不正确的是( )
溶解度曲线为我们定量描述物质的溶解性供了便利.请你根据如图溶解度曲线判断下列说法,其中不正确的是( )