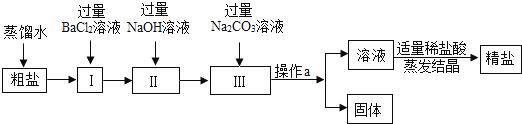
题目内容
【题目】根据下列装置图,回答有关问题: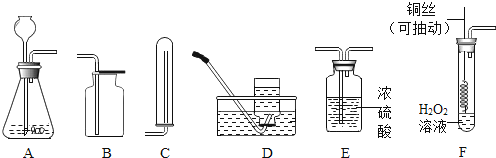
(1)实验室用过氧化氢制取氧气的化学方程式为 ,若要制取并收集一瓶干燥的氧气,应选用装置的连接顺序为 (选填字母),检验氧气是否收集满的方法为 .
(2)实验室常用锌粒和稀硫酸反应制取氢气,有关反应的化学方程式为 .若用排空气法收集,应选用的收集装置为 (选填字母).
(3)实验改进:查阅资料发现,氧化铜可以用作过氧化氢分解制氧气的催化剂.现有一根洁净的铜丝,实验前先将其绕成螺旋状,再经过处理.改进后的发生装置如图F所示(己略去夹持装置).
①铜丝绕成螺旋状的作用是 .
A.收集到更多的O2 B.加快反应速率 C.没有影响
②与装置A比较,改进后装置的优点是 .
【答案】
(1)2H2O2![]() 2H2O+O2↑;A、E、B;用一根带火星的木条放在集气瓶口
2H2O+O2↑;A、E、B;用一根带火星的木条放在集气瓶口
(2)Zn+H2SO4=ZnSO4+H2↑;C
(3)灼烧;B;可随时控制反应的进行
【解析】(1)过氧化氢在二氧化锰的催化作用下分解为水和氧气;因为反应物是固体与液体,在常温下进行,选择装置A来制取,收集一瓶干燥的氧气,用浓硫酸来进行干燥,用向上排空气法来收集;氧气验满时,可将一根带火星的木条放在集气瓶口,观察木条是否复燃;故填:2H2O2![]() 2H2O+O2↑;A、E、B;用一根带火星的木条放在集气瓶口;
2H2O+O2↑;A、E、B;用一根带火星的木条放在集气瓶口;
(2)锌和稀硫酸反应生成硫酸锌和氢气,因为氢气的密度比空气小,所以可用向下排空气法来收集;故填:Zn+H2SO4=ZnSO4+H2↑;C;
(3)将铜丝灼烧,铜与氧气反应生成氧化铜;故填:灼烧;
①将铜丝绕成螺旋状,增大了与反应物的接触面积,加快了反应的速率;故填:B;
②改进后的装置,通过抽动铜丝来控制反应的发生和停止;故填:可随时控制反应的进行.
【考点精析】根据题目的已知条件,利用氧气的化学性质和氧气的检验和验满的相关知识可以得到问题的答案,需要掌握氧气的化学性质:特有的性质:支持燃烧,供给呼吸;氧气的验满:用带火星的木条放在集气瓶口;检验:用带火星的木条伸入集气瓶内.