题目内容
|
某校化学兴趣小组参观制碱厂后获得以下信息,并对相关问题进行研究。 | ||||||
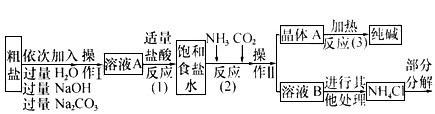 | ||||||
| 上述流程中涉及的部分反应的化学方程式为:MgCl2+2NaOH==Mg(OH)2↓ +2NaCl;Na2CO3+CaCl2==CaCO3↓+2NaCl;NH4Cl==NH3↑+HCl↑。生产原理:将氨气(NH3)和二氧化碳通入饱和食盐水中得到小苏打和氯化铵的混合物,其反应的化学方程式为:NaCl(饱和溶液)+NH3+CO2+H2O==NaHCO3(晶体)↓+NH4Cl4分离出NaHCO3,使其充分受热即可分解制得纯碱及两种常见的氧化物,此反应的化学方程式为______________________________________________。 【问题讨论】(2)溶液A中的溶质为________,操作Ⅱ的名称为_____________。 (3)上述生产流程中可循环使用的是____ (填序号)。 A.CO2;B.NH3;C.HCl;D.NaOH;E.Na2CO3 (4)根据上述信息,请你设计实验区分碳酸钠和碳酸氢钠: | ||||||
| ||||||
|
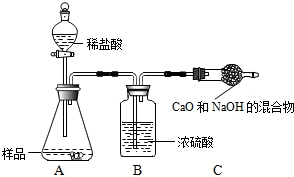
【含量测定】同学们为了测定该纯碱样品的纯度,设计了如下实验。 | ||||||
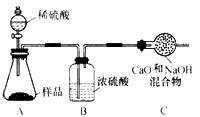 |
| (1)Na2CO3;2NaHCO3==Na2CO3+H2O+CO2↑ 【问题讨论】(2) NaCl、NaOH、Na2CO3;过滤 (3)ABCE (4)  【含量测定】86. 7%;生成的二氧化碳气体没有被C中的烧碱完全吸收 |

练习册系列答案
相关题目
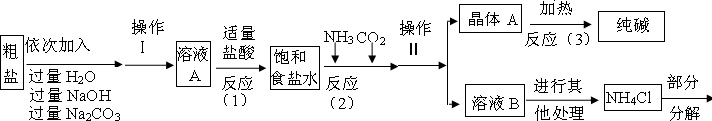
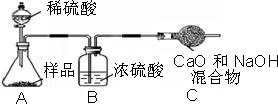 小心蒸发,并将所得物质干燥、冷却至室温后称得固体质量为13.1g.样品中碳酸钠的质量分数为
小心蒸发,并将所得物质干燥、冷却至室温后称得固体质量为13.1g.样品中碳酸钠的质量分数为