题目内容
(2011?杨浦区二模)用某种粗盐进行提纯实验,步骤如图所示.
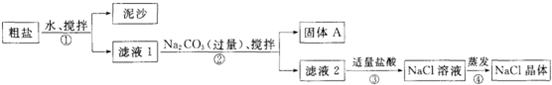
请回答下列问题:
(1)步骤①和②的操作名称是
(2)步骤④加热蒸发时要用到玻璃棒不断搅拌,这是为了防止
(3)猜想和验证:

请回答下列问题:
(1)步骤①和②的操作名称是
过滤
过滤
.(2)步骤④加热蒸发时要用到玻璃棒不断搅拌,这是为了防止
溶液局部过热而飞溅
溶液局部过热而飞溅
.(3)猜想和验证:
| 猜 想 | 验证方法 | 实验现象 | 结 论 |
| 猜想l:固体A中含CaCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | 产生气泡,烧杯内壁有白色固体生成 产生气泡,烧杯内壁有白色固体生成 |
猜想l成立 |
| 猜想Ⅱ:固体A中含BaCO3 | 取少量固体A于试管中,先滴入 盐酸或硝酸 盐酸或硝酸 ,再滴入Na2SO4溶液 |
有气泡放出,无白色沉淀 | 猜想Ⅱ不成立 猜想Ⅱ不成立 |
| 猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量NaCl晶体于试管中,加 适量蒸馏水溶解,再 加BaCl2或Ba(NO3)2 加BaCl2或Ba(NO3)2 |
溶液有白色沉淀生成 溶液有白色沉淀生成 |
猜想Ⅲ成立 |
分析:(1)粗盐提纯实验的步骤为:溶解→过滤→蒸发结晶,过滤时的注意事项:“一贴,二低,三靠”,如有违反可能引起的误差;
(2)蒸发结晶时,注意:用玻璃棒的不断搅拌作用,防止局部过热,造成固体(或溶液)飞溅;
(3)①猜想Ⅰ成立,稀盐酸和碳酸盐反应生成二氧化碳,气体会使澄清石灰水变浑浊;②猜想Ⅱ成立的话,硫酸根会和钡离子形成白色沉淀,且不溶于硝酸;猜想Ⅲ成立时加可溶性的钡盐会产生白色沉淀.
(2)蒸发结晶时,注意:用玻璃棒的不断搅拌作用,防止局部过热,造成固体(或溶液)飞溅;
(3)①猜想Ⅰ成立,稀盐酸和碳酸盐反应生成二氧化碳,气体会使澄清石灰水变浑浊;②猜想Ⅱ成立的话,硫酸根会和钡离子形成白色沉淀,且不溶于硝酸;猜想Ⅲ成立时加可溶性的钡盐会产生白色沉淀.
解答:解:(1)粗盐提纯步骤为:溶解→过滤→蒸发结晶,分离固体和液体时的操作为过滤,故答案为:过滤;
(2)蒸发结晶时,注意:用玻璃棒不断搅拌,防止局部过热,造成固体(或溶液)飞溅,故答案为:溶液局部过热而飞溅;
(3)猜想Ⅰ成立,稀盐酸和碳酸钙反应生成二氧化碳,二氧化碳气体会使澄清石灰水变浑浊;猜想Ⅱ:碳酸钡能被酸溶解,检验钡离子的方法是加入可溶性的硫酸盐,产生不溶于硝酸的白色沉淀;猜想Ⅲ成立时,加可溶性的钡盐来检验硫酸根的存在,会产生白色沉淀,故答案为:猜想Ⅰ:产生气泡,烧杯内壁有白色固体生成;猜想Ⅱ:盐酸或硝酸;猜想Ⅱ不成立;猜想Ⅲ:加BaCl2或Ba(NO3)2;溶液有白色沉淀生成.
(2)蒸发结晶时,注意:用玻璃棒不断搅拌,防止局部过热,造成固体(或溶液)飞溅,故答案为:溶液局部过热而飞溅;
(3)猜想Ⅰ成立,稀盐酸和碳酸钙反应生成二氧化碳,二氧化碳气体会使澄清石灰水变浑浊;猜想Ⅱ:碳酸钡能被酸溶解,检验钡离子的方法是加入可溶性的硫酸盐,产生不溶于硝酸的白色沉淀;猜想Ⅲ成立时,加可溶性的钡盐来检验硫酸根的存在,会产生白色沉淀,故答案为:猜想Ⅰ:产生气泡,烧杯内壁有白色固体生成;猜想Ⅱ:盐酸或硝酸;猜想Ⅱ不成立;猜想Ⅲ:加BaCl2或Ba(NO3)2;溶液有白色沉淀生成.
点评:熟记过滤方法及原理、注意事项;学会猜想和验证,会利用一些标志性的特征:硫酸根会和钡离子形成白色沉淀,且不溶于硝酸.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
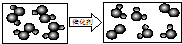
 ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,则如图所示的化学反应方程式为:
”表示氧原子,则如图所示的化学反应方程式为: