题目内容
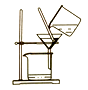
【题目】在化学课上,老师带来一瓶未知溶液A,已知它是稀盐酸或稀硫酸中的一种,进行如下实验(图1):
(1)观察到烧杯值的现象是 .
(2)【提出问题】A是哪一种酸?
老师要求甲、乙同学从反应后的溶液B分别展开探究.
【猜想假设】甲同学:A是稀盐酸;乙同学:A是稀硫酸.
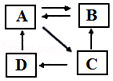
【实验探究】(如图2)
【评价交流】甲同学的实验(填“能”或“不能”)得出正确结论,乙同学的实验(填“能”或“不能”)得出正确结论.
实验3发生反应的化学方程式为 , 反应后所得溶液中一定含有的离子是 .
(3)【归纳总结】通过乙同学的实验可以得出:选择试剂鉴别溶液中的待测离子时,如果待测溶液中含有干扰离子,则应在鉴别前,先另选试剂将干扰离子变成除去.经讨论我们能够总结出,除去溶液中干扰离子的一般方法是:选择试剂将干扰离子变成除去.
【答案】
(1)有气泡冒出
(2)不能;能;BaCl2+Na2SO4═BaSO4↓+2NaCl;NO3﹣、Cl﹣、Na+
(3)气体;沉淀或气体或水
【解析】解:(1)观察到燃烧值的现象是有气泡冒出;故填:有气泡冒出;(2)甲同学的实验中将反应后的溶液中加入硝酸银溶液后生成白色沉淀,就认定A为稀盐酸,其实因为反应后的溶液中有碳酸根离子,生成的白色沉淀是碳酸银,故不能证明A为稀盐酸;故填:不能;(3)乙同学的实验中先在反应后的溶液中加入稀硝酸,把碳酸根离子除去,然后加入氯化钡溶液,生成白色沉淀硫酸钡,从而证明A为稀硫酸,过程正确,能得出正确结论;故填:能;(4)在实验3中的反应物是氯化钡和硫酸钠,反应生成硫酸钡和氯化钠,其反应的化学方程式为:BaCl2+Na2SO4═BaSO4↓+2NaCl;(5)由实验及反应物、生成物可知,反应后的溶液中由硝酸根离子、钠离子和氯离子;故填:NO3﹣;Cl﹣;Na+;(6)选择试剂鉴别溶液中的待测离子时,如果待测溶液中含有干扰离子,则应在鉴别前,先另选试剂将干扰离子除去,该实验中,乙同学先将干扰离子碳酸根离子变成了气体除掉;而在选择除去干扰离子的做法中,要考虑的是把干扰离子变成沉淀、气体或水,这样都能把干扰离子除掉;故填:气体;沉淀或气体或水;
【考点精析】解答此题的关键在于理解书写化学方程式、文字表达式、电离方程式的相关知识,掌握注意:a、配平 b、条件 c、箭号.

 天天练口算系列答案
天天练口算系列答案