题目内容
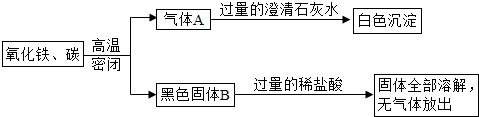
(2013?东城区二模)如图所示的实验中,反应前氧化铁和碳粉的质量分别为16克和0.6克,反应后得到气体A和14.4克黑色固体B.
(1)计算白色沉淀的质量;
(2)通过计算推断黑色固体B的化学式.

(1)计算白色沉淀的质量;
(2)通过计算推断黑色固体B的化学式.
分析:(1)根据质量守恒定律,由反应前氧化铁和碳粉的质量,反应后得到黑色固体B的质量可以计算出得到气体A的质量,进而根据反应的化学方程式计算出生成白色沉淀的质量.
(2)根据现象:黑色固体B与过量的稀盐酸反应生成固体全部溶解,说明B中不含碳;无气体放出,说明不含金属铁;据此根据质量守恒定律进行分析推断.
(2)根据现象:黑色固体B与过量的稀盐酸反应生成固体全部溶解,说明B中不含碳;无气体放出,说明不含金属铁;据此根据质量守恒定律进行分析推断.
解答:解:(1)由题意可知,生成的气体A是二氧化碳,生成二氧化碳的质量=16g+0.6g-14.4g=2.2g
设生成白色沉淀的质量为x
CO2+Ca(OH)2=CaCO3↓+H2O
44 100
2.2g x
根据:
=
解得x=10g
(2)根据现象判断黑色固体没有铁和碳.
氧化铁中含铁元素的质量=16g×
×100%=11.2g;
根据反应前后元素种类不变,则B中铁元素的质量为11.2g,则黑色固体B中含氧元素的质量=14.4g-11.2g=3.2g
若固体B的化学式为FexOy,由化合物中原子的个数比=
则x:y=
:
=1:1;
所以固体B的化学式为:FeO.
故答案为:(1)10g;(2)FeO.
设生成白色沉淀的质量为x
CO2+Ca(OH)2=CaCO3↓+H2O
44 100
2.2g x
根据:
| 44 |
| 100 |
| 2.2g |
| x |
(2)根据现象判断黑色固体没有铁和碳.
氧化铁中含铁元素的质量=16g×
| 56×2 |
| 56×2+16×3 |
根据反应前后元素种类不变,则B中铁元素的质量为11.2g,则黑色固体B中含氧元素的质量=14.4g-11.2g=3.2g
若固体B的化学式为FexOy,由化合物中原子的个数比=
| 元素质量比 |
| 相对原子质量比 |
| 11.2g |
| 56 |
| 3.2g |
| 16 |
所以固体B的化学式为:FeO.
故答案为:(1)10g;(2)FeO.
点评:本题难度较大,考查根据化学方程式的计算、化学式的推断及灵活运用所学知识进行分析解题的能力.

练习册系列答案
相关题目