题目内容
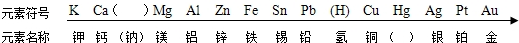
(1)请在上图( )里填上适当的元素符号或元素名称______.
(2)已知置换反应:A+B→C+D能够发生.
①若D为H2,B为稀硫酸,则A的选择应满足的条件是______,
②若D为Cu,写出一个符合该条件的化学方程式______.
(3)下列事实不能说明Zn比Ag活泼的是(______)
A.Zn能与AgNO3溶液反应,置换出Ag
B.Zn能与稀硫酸反应,Ag则不能
C.自然界没有以单质形式存在的Zn,而有以单质形式存在的Ag
D.Zn的熔点为420℃,Ag的熔点为962℃
(4)实验室现有下列药品:盐酸(5%)、硫酸(5%);大小相同的镁片、铝片、铁片;铁粉、铝粉.某同学为了比较金属与酸的反应,按如图所示的实验方案进行实验.
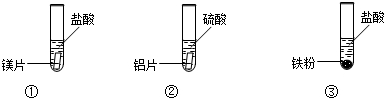
从实验开始到反应5分钟,所观察到的现象记录如下:
| 编号 | ① | ② | ③ |
| 现象 | 金属表面立即有大量无色气泡冒出,反应不到5分钟金属已消失 | 金属表面慢慢有少量无色气泡冒出,反应到5分钟时,铝片上还在冒气泡 | 铁粉中不断有无色气泡冒出,气泡量比②中多,溶液逐渐显浅绿色,反应到5分钟时,铁粉还在冒气泡 |
你认为该同学的结论是否合理(填“合理”或“不合理)______.理由是______.
故答案为:Na,汞;
(2)①能与硫酸发生置换反应生成氢气的金属,其活动性应在金属活动性顺序表中处于H之前;
故答案为:在金属活动性顺序中位于氢前面的金属;
②有铜生成的置换反应主要有两类反应:其一为活泼金属与可溶性铜盐的反应,其二为木炭、氢气还原氧化铜的反应;
故答案为:Fe+CuSO4=FeSO4+Cu(其它合理答案也正确);
(3)通过金属与酸的反应、金属与盐溶液的反应都可以证明两种金属的活动性;金属在自然界中存在形式也与金属活动性有一定关系:活泼金属很难以单质形式存在;而金属的活动性与金属熔点高低无关;
故选D;
(4)为探究金属的活动性,在进行实验时没有控制金属的形状,金属因与酸接触不同而出现反应速度上的差异不能准确体现金属的活动性,所以该同学的操作与所得结论不合理;
故答案为:不合理;只有在相同条件下才有可比性(如金属镁、铁、铝均应为片状的或粉末状,酸应为稀盐酸或稀硫酸中的同一种),它们所用的金属形状不同且酸也不是同一种.

 科学实验活动册系列答案
科学实验活动册系列答案(9分)金属的活泼性顺序排列如下:
元素符号 K Ca()Mg Al Zn Fe Sn Pb (H) Cu(Hg)Ag Pt Au
 |
元素名称钾钙(钠)镁铝锌铁锡铅氢铜( )银铂金
(1)请在上图()里填上适当的元素符号或元素名称
(2)已知置换反应:A + B → C + D 能够发生。
①若D为H2,B为稀硫酸,则A的选择应满足的条件是 ,
②若D为Cu,写出一个符合该条件的化学方程式 。
(3)下列事实不能说明Zn比Ag活泼的是( )
A.Zn能与AgNO3溶液反应,置换出Ag
B.Zn能与稀硫酸反应,Ag则不能
C.自然界没有以单质形式存在的Zn,而有以单质形式存在的Ag
D.Zn的熔点为420℃,Ag的熔点为962℃
(4)实验室现有下列药品:盐酸(5%)、硫酸(5%);大小相同的镁片、铝片、铁片;铁粉、铝粉。某同学为了比较金属与酸的反应,按下图所示的实验方案进行实验。

从实验开始到反应5分钟,所观察到的现象记录如下:
| 编号 | ① | ② | ③ |
| 现象 | 金属表面立即有大量无色气泡冒出,反应不到5分钟金属已消失 | 金属表面慢慢有少量无色气泡冒出。反应到5分钟时,铝片上还在冒气泡 | 铁粉中不断有无色气泡冒出。气泡的量比②中多,溶液逐渐显浅绿色,反应到5分钟时,铁粉还在冒气泡 |
你认为该同学的结论是否合理(填“合理”或“不合理)_______________。理由是
。
金属的活泼性顺序排列如下:
元素符号 K Ca( )Mg Al Zn Fe Sn Pb (H) Cu(Hg)Ag Pt Au
元素名称 钾 钙(钠)镁铝锌铁 锡 铅 氢 铜( )银 铂 金
(1)请在上图( )里填上适当的元素符号或元素名称
(2)已知置换反应:A + B → C + D 能够发生。
①若D为H2,B为稀硫酸,则A的选择应满足的条件是 ,
②若D为Cu,写出一个符合该条件的化学方程式 。
(3)下列事实不能说明Zn比Ag活泼的是( )
A.Zn能与AgNO3溶液反应,置换出Ag
B.Zn能与稀硫酸反应,Ag则不能
C.自然界没有以单质形式存在的Zn,而有以单质形式存在的Ag
D.Zn的熔点为420℃,Ag的熔点为962℃
(4)实验室现有下列药品:盐酸(5%)、硫酸(5%);大小相同的镁片、铝片、铁片;铁粉、铝粉。某同学为了比较金属与酸的反应,按下图所示的实验方案进行实验。

从实验开始到反应5分钟,所观察到的现象记录如下:
|
编号 |
① |
② |
③ |
|
现象 |
金属表面立即有大量无色气泡冒出,反应不到5分钟金属已消失 |
金属表面慢慢有少量无色气泡冒出。反应到5分钟时,铝片上还在冒气泡 |
铁粉中不断有无色气泡冒出。气泡的量比②中多,溶液逐渐显浅绿色,反应到5分钟时,铁粉还在冒气泡 |
该同学根据上述实验现象得出结论:金属与酸反应的剧烈程度按镁、铁、铝的顺序减弱。
你认为该同学的结论是否合理(填“合理”或“不合理)_______________。理由是
。

(1)请在上图( )里填上适当的元素符号或元素名称 .
(2)已知置换反应:A+B→C+D能够发生.
①若D为H2,B为稀硫酸,则A的选择应满足的条件是 ,
②若D为Cu,写出一个符合该条件的化学方程式 .
(3)下列事实不能说明Zn比Ag活泼的是( )
A.Zn能与AgNO3溶液反应,置换出Ag
B.Zn能与稀硫酸反应,Ag则不能
C.自然界没有以单质形式存在的Zn,而有以单质形式存在的Ag
D.Zn的熔点为420℃,Ag的熔点为962℃
(4)实验室现有下列药品:盐酸(5%)、硫酸(5%);大小相同的镁片、铝片、铁片;铁粉、铝粉.某同学为了比较金属与酸的反应,按如图所示的实验方案进行实验.

从实验开始到反应5分钟,所观察到的现象记录如下:
| 编号 | ① | ② | ③ |
| 现象 | 金属表面立即有大量无色气泡冒出,反应不到5分钟金属已消失 | 金属表面慢慢有少量无色气泡冒出,反应到5分钟时,铝片上还在冒气泡 | 铁粉中不断有无色气泡冒出,气泡量比②中多,溶液逐渐显浅绿色,反应到5分钟时,铁粉还在冒气泡 |
你认为该同学的结论是否合理(填“合理”或“不合理) .理由是 .


