题目内容
【题目】化学是以实验为基础的科学,实验是科学探究的重要手段。47 中某化学兴趣小组在一次活动中 想选择一种试剂鉴别 “稀盐酸、氯化钠溶液和澄清石灰水”。现将三种无色溶液分别标记为A、B、C。
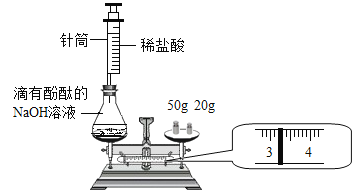
[实验探究1]:甲同学认为可以选择一种有色溶液鉴别,他选择的试剂为_____,乙同学选择用碳酸钠溶液鉴别,实验如图所示:
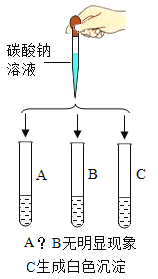
A试管中发生反应的化学方程式为_____。
实验结束后,乙同学先将B试管溶液倒入废液缸,再将A试管溶液倒入废液缸,观察到有气泡冒出,最后将C试管滤液倒入废液缸时,立即产生白色沉淀,则C试管滤液中含有的阳离子为_____。
[实验探究2]:对上述反应后的废液进行过滤,同学们对上述滤液中的溶质成分产生了兴趣。
[提出问题]:反应后的溶液中含有哪些溶质呢?
[猜想与假设]:
小峰同学认为溶质是: NaCl、 NaOH 、Na2CO3
小马同学认为溶质是: NaCl、NaOH
小谢同学认为溶质是: NaCl 、Na2CO3、 Ca(OH)2
[交流与评价]:经讨论小谢同学的猜想一定不正确, 理由是_____。
[活动与探究]小峰同学想证明自己的猜想正确,于是他取滤液少许,向其中加入足量的稀盐酸,却未观察到气泡,于是他得出结论:自己的猜想错误,小马同学的猜想是正确的。请对小峰同学的结论进行评价_____。最后经过同学们合作探究最终证明了溶质的成分。现在小瀛同学带领小组同学一起讨论,此滤液在排放前应如何进行处理,讨论的结果是_____。
[总结与提升]通过上述实验,若用一种试剂一次性鉴别多种物质时,要求加入的试剂_____。
【答案】石蕊试液 Na2CO3+2HCl=2NaCl+H2O+CO2↑ Na+、Ca2+ Na2CO3与Ca(OH)2不能共存 小峰同学的结论不正确,因为溶液中含有氢氧化钠,如果加入的稀盐酸不足以和氢氧化钠反应,即使溶液中含有碳酸钠,也不产生气泡 加入盐酸,将溶液的pH调至中性,再排放 产生不同现象
【解析】
[实验探究1]
甲同学认为可以选择一种有色溶液鉴别,他选择的试剂为石蕊试液,这是因为加入石蕊试液时,无明显现象的是氯化钠溶液,溶液变红色的是稀盐酸,溶液变蓝色的是氢氧化钙溶液;
B试管中无明显现象,说明B溶液是氯化钠溶液,C试管中产生白色沉淀,说明C溶液是氢氧化钙溶液,则A溶液是稀盐酸,稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
结束后,乙同学将B试管溶液倒入废液缸,再将A试管溶液倒入废液缸,观察到有气泡冒出,说明A中稀盐酸过量,B中碳酸钠过量,最后将C试管滤液倒入废液缸时,立即产生白色沉淀,说明A和B的废液反应后碳酸钠过量,C中氢氧化钙过量,则C试管滤液中的溶质有碳酸钠和氢氧化钙反应生成的氢氧化钠和过量的氢氧化钙。阳离子为Na+、Ca2+;
[实验探究2]:
[交流与评价]:
经讨论小谢同学的猜想一定不正确, 理由是Na2CO3与Ca(OH)2生成碳酸钙和氢氧化钠,即Na2CO3与Ca(OH)2不能共存;
[活动与探究]
小峰同学的结论不正确,因为溶液中含有氢氧化钠,如果加入的稀盐酸不足以和氢氧化钠反应,即使溶液中含有碳酸钠,也不产生气泡;
最后经过同学们合作探究最终证明了溶质的成分,溶液中一定存在NaCl、NaOH可能存在Na2CO3,此滤液在排放前应如何进行处理,讨论的结果是加入盐酸,将溶液的pH调至中性,再排放;
[总结与提升]通过上述实验,若用一种试剂一次性鉴别多种物质时,要求加入的试剂产生不同现象。